题目内容
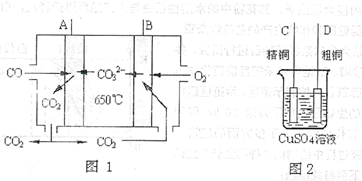
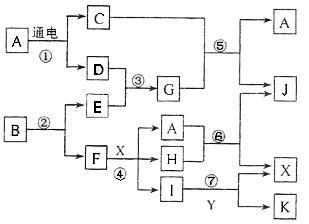
下图中,①②⑤是工业生产上的重要反应,其中反应⑤是合成氨工业的反应,常温下D、F、H、I是气体,B、F、I属单质,固体E与水反应能生成含碳质量分数最高的常见气态烃、固体G俗称石灰氮,由三种元素组成,其相对分子质量小于100,其中含钙元素50.00%、碳占15.00%(图中部分反应物或生成物没有列出)。
请按要求回答:
(1)写出A的化学式______________,H的电子式______________。
(2)反应⑤进行的条件是______________________________。
(3)将少量的D气体通入足量的NaOH溶液的离子反应方程式为______________________________。
(4)反应③的化学方程式为_______________。
(1)CaCO3 
(2)高温、高压、催化剂
(3)CO2+2OH-====![]() +H2O
+H2O
(4)CaC2+N2====CaCN2+C
解析:本题是元素化合物之间的框图推断题,解题关键是E与水反应放出乙炔的是碳化钙,A、B、C、D是CaCO3、C、CaO、CO2。反应(5)是合成氨工业,E是CaC2,G是石灰氮,F是N2,I是H2,J分解生成H2、NH3和单质I2,是NH4I。

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目
(6分)请根据题目要求回答下列问题:
(1)工业接触法制硫酸的生产中用到的设备有:①沸腾炉② ,
③吸收塔,写出设备②中,发生的主要反应的化学方程式 。
(2)已知SO2转化为SO3的反应为放热反应,下图中正确的是 (填序号)。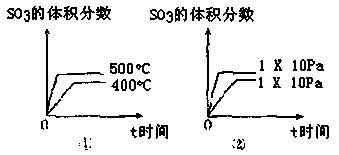
(3)在吸收塔中,为了提高SO3的吸收率,工业上选择的吸收剂是 (填序号)。
| A.H2O | B.稀H2SO4 |
| C.98.3%H2SO4 | D.NH3·H2O溶液 |




 (3)工业上用一氧化碳制取氢气的反应为:CO(g)+H2O CO2(g)+H2(g),已知420℃时,该反应的化学平衡常数为9.0。如果反应开始时,在2L的密闭容器中充入CO和H2O的物质的量都是0.60mol,5min末达到平衡,则此时CO的转化率为
,H2的平均生成速率为
。
(3)工业上用一氧化碳制取氢气的反应为:CO(g)+H2O CO2(g)+H2(g),已知420℃时,该反应的化学平衡常数为9.0。如果反应开始时,在2L的密闭容器中充入CO和H2O的物质的量都是0.60mol,5min末达到平衡,则此时CO的转化率为
,H2的平均生成速率为
。