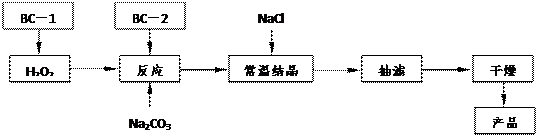题目内容
在1L1mol·L-1 NaOH溶液中通入16.8L标准状况下的CO2,充分反应后判断所得溶液的溶质为何物及计算所得溶液中含有溶质物质的量浓度(设反应后,溶液的体积仍为1L)。
生成物溶质为Na2CO3和NaHCO3,
含有溶质物质的量浓度:
Na2CO3为0.25mol·L-1,
NaHCO3为0.5 mol·L-1。
把CO2通入NaOH溶液中发生的反应有:
2NaOH+CO2 Na2CO3+H2O ①
Na2CO3+H2O ①
NaOH+CO2 NaHCO3 ②
NaHCO3 ②
当n(NaOH)∶n(CO2)≥2∶1时生成物为Na2CO3;n(NaOH)∶n(CO2)≤1∶1时,生成物为NaHCO3,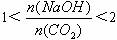 时,生成物既有Na2CO3也有NaHCO3。
时,生成物既有Na2CO3也有NaHCO3。
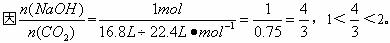
所以生成物既有Na2CO3也有NaHCO3。
2NaOH+CO2
 Na2CO3+H2O ①
Na2CO3+H2O ①NaOH+CO2
 NaHCO3 ②
NaHCO3 ②当n(NaOH)∶n(CO2)≥2∶1时生成物为Na2CO3;n(NaOH)∶n(CO2)≤1∶1时,生成物为NaHCO3,
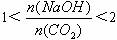 时,生成物既有Na2CO3也有NaHCO3。
时,生成物既有Na2CO3也有NaHCO3。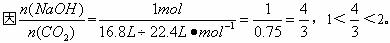
所以生成物既有Na2CO3也有NaHCO3。

练习册系列答案
相关题目