题目内容
设NA表示阿伏加德罗常数的值,下列叙述中正确的是
| A.常温下,1 mol Cl2与足量NaOH溶液完全反应,转移的电子数2NA |
| B.常温常压下,11.2 L CO2中含有的分子数是0.5NA |
| C.标准状况下,22.4 L水所含原子数为3NA |
| D.常温常压下,48 g O3和O2的混合气体中氧原子数为3NA |
D
解析试题分析:A、1 mol Cl2与足量NaOH溶液完全反应,氯气既作氧化剂又作还原剂,所以转移的电子数为NA,错误;B、22.4L/mol的使用条件是标准状况下的气体,常温常压下,11.2LCO2的物质的量不为0.5mol,错误;C、标准状况下的水不为气态,所以标准状况下,22.4 L水的物质的量不是1mol,错误;D、48g的O3和O2的混合气体氧原子的物质的量为48g/16g/mol=3mol,所以常温常压下,48 g O3和O2的混合气体中氧原子数为3NA,正确,答案选D。
考点:考查阿伏伽德罗常数的理解应用

练习册系列答案
相关题目
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A.1L1mol/L的NaClO溶液中含有氧原子的数目为NA |
| B.1L1mol/L的盐酸中含有NA个HCl分子 |
| C.常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA |
| D.加热33.6gNaHCO3至没有气体放出时,转移的电子数目为0.4 NA |
某盐的混合物中含有0.2 mol/L Na+、0.4 mol/L Mg2+、0.4 mol/L Clˉ,则SO42ˉ为
| A.0.1 mol/L | B.0.2 mol/L | C.0.3 mol/L | D.0.4 mol/L |
对1 mol·L-1的BaCl2溶液的有关叙述中,正确的是( )
| A.该溶液中Cl-浓度为2 mol·L-1 |
| B.该溶液中Ba2+的物质的量是1 mol |
| C.可使用250 mL容量瓶分两次完成490 mL该浓度的BaCl2溶液的配制 |
| D.将208 g BaCl2固体溶解在1 L水中,形成的溶液的浓度为1 mol·L-1 |
下列条件下,两种气体分子数一定不相等的是( )
| A.相同质量、不同密度的N2O和CO2 |
| B.相同体积、相同密度的CO和C2H4 |
| C.相同温度、相同压强、相同体积的O2和O3 |
| D.相同压强、相同体积、相同质量的NO2和N2O4 |
把500 mL NH4HCO3和Na2CO3的混合溶液分成五等份,取一份加入含a mol氢氧化钠的溶液恰好反应完全,另取一份加入含b mol HCl的盐酸恰好反应完全,则该混合溶液中c(Na+)为( )
A.(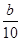 - -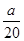 ) mol/L ) mol/L | B.(2b-a) mol/L |
C.(5b-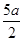 ) mol/L ) mol/L | D.(10b-5a) mol/L |
有一瓶14%的KOH溶液,加热蒸发掉100 g水后,变为28%的KOH溶液80 mL,该80 mL溶液的物质的量浓度为( )
| A.5 mol/L | B.6 mol/L |
| C.6.25 mol/L | D.6.75 mol/L |
实验室中需要0.2 mol·L-1的NaOH溶液65 mL,配制该溶液时应选用的容量瓶的规格和称取的NaOH质量分别是( )。
| A.65 mL,0.52 g | B.70 mL,0.56 g |
| C.100 mL,0.52 g | D.100 mL,0.8 g |
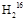 O与80 g
O与80 g 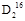 O的物质的量之比是 ,分子中所含质子数之比是 ,所含中子数之比是 ,它们分别与Na反应时,所放出气体体积之比(同条件)是 ,质量之比是 。
O的物质的量之比是 ,分子中所含质子数之比是 ,所含中子数之比是 ,它们分别与Na反应时,所放出气体体积之比(同条件)是 ,质量之比是 。