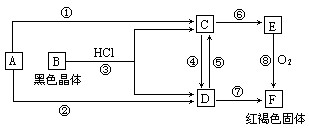
题目内容
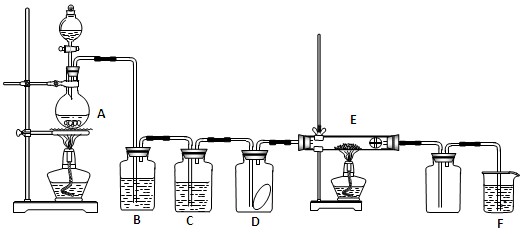
(10分)下图为实验室制取纯净、干燥的Cl2,并进行检验Cl2性质实验的装置。其中D瓶中放有干燥红色布条;E中为铜网,E右端出气管口附近为石棉球。
试回答:
(1)A中发生反应的方程式为_____________ _________________________________;
(2)为得到干燥纯净的氯气,一般在B瓶中加入饱和食盐水,其作用是______________;
(3)C中盛放的试剂为_____________;
(4)E中所发生反应的方程式为____________________________________________。
(5) F中应加入的试剂为 ,其作用是 。
(6)若A中有14.6g HCl 被氧化,将产生的氯气通入足量的KI溶液中能产生单质碘的质量 为_____________g。
MnO2 +4HCl(浓)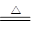 MnCl2 + Cl2↑ + 2H2O ;吸收HCl气体;浓H2SO4;
MnCl2 + Cl2↑ + 2H2O ;吸收HCl气体;浓H2SO4;
Cu + Cl2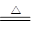 CuCl2 ;碱液;吸收多余的氯气;50.8 g
CuCl2 ;碱液;吸收多余的氯气;50.8 g
解析

(10分)下表是某超市出售的加碘食盐的有关说明:
| 配 料 表 | 精制盐、碘酸钾 |
| 含 碘 量 | 45±5mg/kg |
| 储 藏 方 法 | 通风、防潮 |
| 食 用 方 法 | 根据烹调所需适量加入 |
某研究性学习小组欲通过实验检验该碘盐中是否含碘:
(1)首先取该食盐样品配制室温下的饱和溶液:向200mL蒸馏水中加入75.0g 该食盐样品,加热并搅拌,直到完全溶解。冷却至室温。(已知室温条件下氯化钠溶解度为36 g)
在加热过程中需要用到的仪器有铁架台、酒精灯、铁圈、____________、烧杯和玻璃棒。冷却至室温过程中若出现____________________(填现象),则证明其为饱和溶液。
(2)甲同学先向该饱和食盐溶液中加入1mol/L的KI溶液和几滴淀粉溶液,然后加入0.1mol/L稀硫酸,振荡,溶液变为蓝色。该实验发生的化学反应中氧化剂与还原剂的物质的量之比为_______________。请在下图中画出参加反应的IO3—的物质的量和析出的I2单质的物质的量的关系曲线。
(3)乙同学认为甲同学的实验方案不严谨,他提出如下假设:空气中的氧气可能参与反应,使溶液变蓝。反应的离子方程式为:_____________________________________。
请你设计实验方案验证乙同学的假设是否正确:
。