题目内容
12.电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用.阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用.某科研小组用电浮选凝聚法处理污水,设计装置示意图,如图所示.下列说法正确的是( )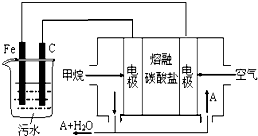
| A. | Fe为阳极,其电极反应为:Fe-3e-+3OH-=Fe(OH)3↓ | |
| B. | 通入甲烷的电极为负极,其电极反应为:CH4-8e-+10OH-=CO32-+7H2O | |
| C. | 为了使该燃料电池长时间稳定运行,电池工作时必须 有部分A物质参加循环.A物质是CO2 | |
| D. | 实验过程中,若在阴极产生了4.48 L气体,则电路中通过的电子个数为0.4NA |
分析 燃料电池中,正极发生的反应是氧气得电子被还原的过程,负极发生的反应是燃料失电子被氧化的过程;电池是以熔融碳酸盐为电解质,可以循环利用的物质只有二氧化碳,甲烷燃料电池中,负极发生的反应是甲烷失电子被氧化的过程,电极反应式为CH4+4CO32--8e-=5CO2+2H2O,所以电解时铁作阳极,因此主要发生Fe-2e-=Fe2+,阴极上氢离子得电子生成氢气,据此分析.
解答 解:A、电解时铁作阳极,因此主要发生Fe-2e-=Fe2+,故A错误;
B、甲烷燃料电池中,负极发生的反应是甲烷失电子被氧化的过程,电极反应式为CH4+4CO32--8e-=5CO2+2H2O,故B错误;
C、电池是以熔融碳酸盐为电解质,可以循环利用的物质只有二氧化碳,使该燃料电池长时间稳定运行,电池工作时必须 有部分A物质参加循环.A物质是CO2,故C正确;
D、电解时阴极反应式为2H++2e-=H2↑,产生4.48 L气体为标准状况下时,转移电子数为0.2NA,故D错误;
故选C.
点评 本题考查原电池和电解池的知识,较为综合,做题时注意利用守恒的思考去解答,同时注意电极反应式的书写.

练习册系列答案
相关题目
9.如表所示,为提纯下列物质(括号内为杂质),所用的除杂试剂和分离方法都正确的是( )
| 序号 | 不纯物 | 除杂试剂 | 分离方法 |
| A | CH4(C2H4) | 酸性KMn04溶液 | 洗气 |
| B | NH4Cl溶液(FeCl3) | NaOH溶液 | 过滤 |
| C | 福尔马林(甲酸) | Na2CO3溶液 | 蒸馏 |
| D | 苯(苯酚) | 溴 水 | 分液 |
| A. | A | B. | B | C. | C | D. | D |
7.反应CH3OH ( l )+NH3( g )═CH3NH2( g )+H2O ( g )在某温度自发向右进行,若反应|△H|=17kJ/mol,|△H-T△S|=17kJ/mol,对于该反应下列关系正确的是( )
| A. | △H>0,△H-T△S<0 | B. | △H<0,△H-T△S>0 | C. | △H>0,△H-T△S>0 | D. | △H<0,△H-T△S<0 |
17.3-氯戊烷是一种有机合成中间体,下列有关3-氯戊烷的叙述正确的是( )
| A. | 3-氯戊烷的分子式为C5H9Cl3 | B. | 3-氯戊烷属于烷烃 | ||
| C. | 3-氯戊烷能发生取代反应 | D. | 3-氯戊烷的同分异构体共有6种 |
4.通常条件下,下列材质的水龙头连接在铁质自来水管上,铁管的腐蚀最快的是( )
| A. | 铁水龙头 | B. | 铜水龙头 | C. | 塑料水龙头 | D. | 铝水龙头 |
1.高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压.高铁电池的总反应为:3Zn+2K2FeO4+8H2O═3Zn(OH)2+2Fe(OH)3+4KOH 下列叙述正确的是( )
| A. | 放电时负极反应为:3Zn-6e-═3Zn2+ | |
| B. | 放电时正极反应为:2FeO42-+6e-+8H2O═2Fe(OH)3+10OH- | |
| C. | 放电时每转移3mol电子,正极有1mol K2FeO4被氧化 | |
| D. | 放电时负极附近溶液的碱性减弱 |
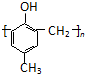 )的合成路线如下:
)的合成路线如下: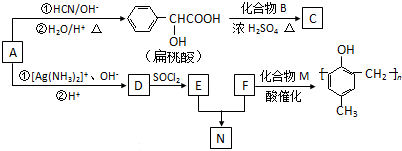
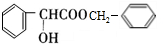 .
. .
.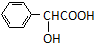 )有多种同分异构体.属于甲酸酯且含酚羟基的同分异构体有13种,写出其中一个含亚甲基(-CH2-)的同分异构体的结构简式
)有多种同分异构体.属于甲酸酯且含酚羟基的同分异构体有13种,写出其中一个含亚甲基(-CH2-)的同分异构体的结构简式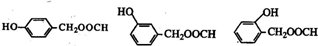 (任意一种).
(任意一种).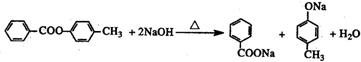 .
.