题目内容
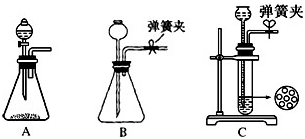
(1)Na2CO3固体中混有少量NaHCO3固体,除去杂质的方法是________,化学方程式是________.
(2)NaHCO3固体中混有少量Na2CO3固体,除杂方法是________,化学方程式是________.
(3)NaOH固体中混有少量Na2CO3固体,除杂方法是________,反应的化学方程式是________.
答案:
解析:
提示:
解析:
|
|
提示:
|
第(2)题反应条件是在水存在时,故需要先将固体溶于水. |

练习册系列答案
 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案
相关题目
 (2010?江苏)高纯MnCO3是制备高性能磁性材料的主要原料.实验室以MnO2为原料制备少量高纯MnCO3的操作步骤如下:
(2010?江苏)高纯MnCO3是制备高性能磁性材料的主要原料.实验室以MnO2为原料制备少量高纯MnCO3的操作步骤如下: