题目内容
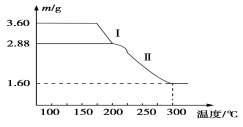
【题目】室温下,将1mol的CuSO4·5H2O(s)溶于水会使溶液温度降低,其过程表示为:CuSO4·5H2O(s) = Cu2+(aq)+SO42-(aq)+5 H2O(l) 热效应为△H1;将 1mol CuSO4(s)溶于水会使溶液温度升高,其过程表示为:CuSO4(s) =Cu2+(aq)+SO42-(aq) 热效应为△H2;CuSO4·5H2O受热分解的化学方程式为:CuSO4·5H2O(s) ![]() CuSO4(s)+5H2O(l),热效应为△H3。则下列判断正确的是( )
CuSO4(s)+5H2O(l),热效应为△H3。则下列判断正确的是( )
A.△H1<△H3 B.△H2>△H3
C.△H1+△H3 =△H2 D.△H1+△H2 >△H3
【答案】A
【解析】
试题分析:根据题意知胆矾溶于水时,溶液温度降低,则反应①:CuSO4·5H2O(s) = Cu2+(aq)+SO42-(aq)+5 H2O(l)的△H1>0;1mol CuSO4(s)溶于水会使溶液温度升高,则反应②:CuSO4(s) =Cu2+(aq)+SO42-(aq) 的△H2<0;又反应③:CuSO4·5H2O(s) =CuSO4(s)+5H2O(l),热效应为△H3;依据盖斯定律①﹣②=③,所以△H3=△H1﹣△H2;△H2<0,△H1>0,则△H3>0。A、分析可知△H2=△H1﹣△H3,由于△H2<0,△H3>△H1,正确;B、上述分析可知△H2<△H3,错误;C、△H2=△H1-△H3,错误;D、△H2<0,△H1>0、△H3>△H1+△H2,错误。

【题目】下列除去杂质的方法中错误的是( )
物质 | 杂质 | 除杂质的方法 | |
A | CaCl2溶液 | HCl | 过量CaCO3、过滤 |
B | NaOH溶液 | Ca(OH)2 | 过量Na2CO3溶液、过滤 |
C | FeCl2溶液 | CuCl2 | 过量铁粉、过滤 |
D | CO2 | H2O | 通过盛浓硫酸的洗气瓶 |
A.A
B.B
C.C
D.D