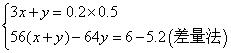题目内容
将6g纯铁粉加入200mL Fe(SO4)3和CuSO4的混合溶液中,充分反应得到200mL 0.5 mol×L-1FeSO4溶液和5.2g固体沉淀物。计算:(1)反应后生成铜多少克?
(2)加入铁粉前,Fe2(SO4)3溶液的物质的量浓度是多少?
答案:
解析:
解析:
| 解:设溶液中有Fe2(SO4)3 x mol、CuSO4 y mol
2Fe3++Fe══3Fe2+,Fe+Cu2+══Fe2++Cu 2x x 3x y y y y
解得:x=0.02mol y=0.04mol Cu:0.04´64g=2.56g Fe(SO4)3物质的量浓度 =
|

练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目