题目内容
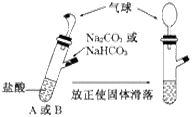
(14分)黄铜矿是工业炼铜的主要原料,其主要成分为CuFeS2,现有一种天然黄铜矿(含少量脉石SiO2),为了测定该黄铜矿的纯度,某同学设计了如下实验:

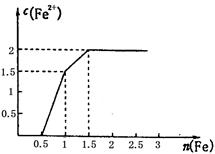
现称取研细的黄铜矿样品1.150 g,在空气存在下进行煅烧,生成Cu、Fe2O3、FeO和SO2气体,实验后取d中溶液的1/10置于锥形瓶中,用0.05000 mol·L-1标准碘溶液进行滴定,初读数为0.10 mL,末读数如右图所示。
(1)冶炼铜的反应为8CuFeS2+ 21O2 高温8Cu + 4FeO + 2Fe2O3+ 16SO2,若CuFeS2中Fe的化合价为+2,反应中被还原的元素是 (填元素符号)。
(2)装置a的作用是 。
| A.有利于空气中氧气充分反应 | B.除去空气中的水蒸气 |
| C.有利于气体混合 | D.有利于观察空气流速 |
(4)滴定时,标准碘溶液所耗体积为 mL。用化学方程式表示滴定的原理: 。
(5)通过计算可知,该黄铜矿的纯度为 。
(1)Cu、O (2分); (2)BD (2分);(3)将系统装置中SO2全部排入d中充分吸收(2分)
(4)20.00 (2分);I2+ SO2+ 2H2O=H2SO4+ 2HI(3分) (5)80.00%(3分)
解析试题分析:(1)若CuFeS2中Fe的化合价为+2,则铜元素和硫元素的化合价分别为+2价和-2价。根据化学方程式可知,反应后铜元素化合价降低,氧元素化合价也降低,硫元素化合价升高,铁元素化合价部分升高,因此反应中被还原的元素是Cu和O。
(2)由于空气中含有水蒸气,因此浓硫酸的作用是干燥空气。另外通过观察a装置中气泡可以控制气体的流速以便于控制反应,故答案为BD。
(3)由于装置还含有未被吸收的SO2,因此继续投入空气的目的是将系统装置中SO2全部排入d中充分吸收。
(4)根据滴定管的液面可知,读数是20.10ml,因此实际消耗标准液的体积为20.10ml-0.10ml=20.00ml。二氧化硫具有还原性,能被碘氧化生成 硫酸,反应的离子方程式为I2+ SO2+ 2H2O=H2SO4+ 2HI。
(5)消耗标准碘的物质的量=0.05000 mol·L-1×0.02000L=0.001000mol,所以根据方程式可知参加反应的二氧化硫的物质的量是0.001000mol,则样品产生的二氧化硫的物质的量是0.001000mol×10=0. 01000mol。因此根据方程式可知CuFeS2的物质的量是0.005ml,质量是0.005ml×184g/mol=0.92g,因此该黄铜矿的纯度为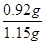 ×100%=80.00%
×100%=80.00%
考点:考查氧化还原反应、实验方案设计、滴定管读数以及物质含量计算

 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案(10分)某研究性学习小组同学向Fe(NO3)3溶液中滴加淀粉KI溶液后,溶液呈蓝色。他们对Fe(NO3)3溶液中将I-氧化的氧化剂进行了如下探究:
【实验】分别向FeCl3溶液和HNO3溶液中滴加淀粉KI溶液后,发现溶液均显蓝色。
(1)FeCl3溶液与KI溶液反应的离子方程式为 。
(2)KI与HNO3反应的离子方程式为I-+H++NO3-→NO↑+I2+H2O(未配平),反应中氧化剂与还原剂的物质的量之比为 。
【提出假设】假设1:氧化剂只有Fe3+ 假设2:氧化剂只有NO3-(H+)
【设计实验方案,验证假设】
(3)请设计实验验证上述假设
供选试剂:0.2mol?L-1的Fe(NO3)3溶液、0.2mol?L-1的KI溶液、0.01mol?L-1的KMnO4酸性溶液、0.01mol?L-1的KSCN溶液、CCl4溶液、淀粉溶液。(提示:NO3-在不同条件下的还原产物较复杂,有时难以观察到气体产生)
| 实验步骤 | 预期现象和结论 |
| ①取5ml0.2mol?L-1的Fe(NO3)3溶液和5ml0.2mol?L-1的KI溶液,充分反应后加入5ml CCl4溶液,振荡静置,取上层溶液,分置于A、B两支试管中 | |
| ② ③ | 若溶液不变红色,则假设1成立,否则假设1不成立; 若溶液显紫色,则假设2成立,否则假设2不成立 |
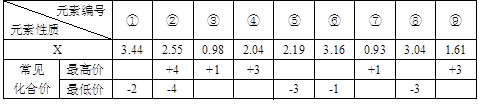
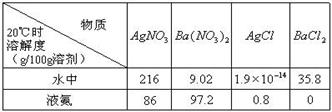
 AsO43-+2I-+ 2H2O,在较强酸性时,上述氧化还原反应向____进行(填:“正反应”或“逆反应”);强碱性时,是否有利H3As3还原I2?为什么?_______________________________________。
AsO43-+2I-+ 2H2O,在较强酸性时,上述氧化还原反应向____进行(填:“正反应”或“逆反应”);强碱性时,是否有利H3As3还原I2?为什么?_______________________________________。

 已知: ,假设测定过程中没有其他反应。根据上述数据,该产品中PCl3的质量分数为 。
已知: ,假设测定过程中没有其他反应。根据上述数据,该产品中PCl3的质量分数为 。