��Ŀ����
����Ŀ����֪���ᡢ�������������Һ�д�������ƽ�⼰���Ӧ��ƽ�ⳣ��
CH3COOH![]() CH3COO-+H+K1=1.75��10-5��H1>0
CH3COO-+H+K1=1.75��10-5��H1>0
CH3COO-+H20![]() CH3COOH+OH-K2=5.71��10-10��H2>0
CH3COOH+OH-K2=5.71��10-10��H2>0
�����£���������������ʵ���Ũ�ȵĴ���ʹ�������Һ��ϣ�����������ȷ����
A. �¶Ȳ���,���ڻ����Һ�м�������NaOH���壬c(CH3COO-)��С
B. �Ի����Һ�����ȣ�K1����K2��С
C. ���ڻ����Һ��pHֵ�����ԣ����ʱ��Һ��c(Na+)>c(CH3COO-)
D. ��֪ˮ�����ӻ�ΪKw�������߹�ϵΪK1��K2=Kw
���𰸡�D
��������A. �¶Ȳ��䣬���ڻ����Һ�м�������NaOH���壬�ᷢ������кͷ�Ӧ��ʹ���ᷢ������ij̶���������c��CH3COO-������A������B. �Ի����Һ�����ȣ���ٽ���ĵ�����ε�ˮ��̶ȣ�����K1����K2Ҳ����B����C. ����Һ�д��ڵ���غ㣺c(H+)��c(Na+)=c(CH3COO-)+c(OH-) �����ڻ����Һ��PHֵ�����ԣ���c(H+)=c(OH-������ʱ��Һ��c(Na+)=c(CH3COO-)����C����D. ![]() ����D��ȷ������ѡD��
����D��ȷ������ѡD��

����Ŀ����ѧ��Ӧԭ���ڹ�ҵ�����о���ʮ����Ҫ�����塣
��1����ҵ����������NH3(g)��CO2(g)��������Ӧ�������أ�������Ӧ�������仯ʾ��ͼ���£�
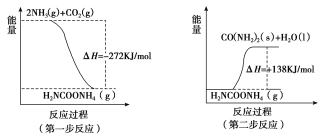
��NH3(g)��CO2(g)��Ӧ�������ص��Ȼ�ѧ����ʽΪ___________________________��
��2����֪��ӦFe(s)��CO2(g) ![]() FeO(s)��CO(g)����H��a kJ��mol��1������ڲ�ͬ�¶��£��÷�Ӧ��ƽ�ⳣ��K���¶ȵı仯���£�
FeO(s)��CO(g)����H��a kJ��mol��1������ڲ�ͬ�¶��£��÷�Ӧ��ƽ�ⳣ��K���¶ȵı仯���£�
�¶�(��) | 500 | 700 | 900 |
K | 1.00 | 1.47 | 2.40 |
�ٸ÷�Ӧ�Ļ�ѧƽ�ⳣ��K�ı���ʽΪ____________��a________0(�>������<������)����500 �� 2 L�ܱ������н��з�Ӧ��Fe��CO2����ʼ����Ϊ4 mol����5 min��ﵽƽ��ʱCO2��ת����Ϊ________������CO��ƽ������v(CO)Ϊ_______________��
��700 �淴Ӧ�ﵽƽ���Ҫʹ��Ӧ����������ƽ�������ƶ��� �ɲ�ȡ�Ĵ�ʩ�� ___________��
��3������CO��H2��ֱ�Ӻϳɼ״�����ͼ���ɡ��״�-�������γɵ���ɫȼ�ϵ�صĹ���ԭ��ʾ��ͼ��д����ʯīΪ�缫�ĵ�ع���ʱ�����ĵ缫��Ӧʽ_____________________�����øõ�ص��1L 0��5mol/L��CuSO4��Һ��������560mLO2����״���£�ʱ��������Һ��pH��_________����Һ���ǰ������ı仯���Բ��ƣ���