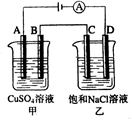
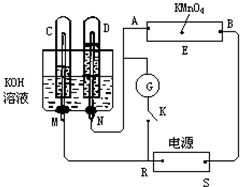
题目内容
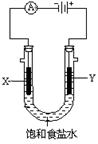
在下图装置中,若通电一段时间后乙装置左侧电极质量增加,则下列说法错误的是( )
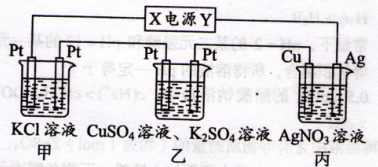

| A.乙中左侧电极反应式:Cu2++2e-=Cu |
| B.电解过程中装置丙的pH无变化 |
| C.向甲中通人适量的HCl气体,可使溶液恢复到电解前的状态 |
| D.当甲装置中产生标准状况下4.48 L气体时,Cu电极上质量增加43.2 g |
D
试题分析:A、乙装置的左侧电极质量增加,则左侧为阴极,由此可确定X极为负极,Y为正极,乙装置中铜离子放电,对;B、装置内阴极析出银单质,阳极上的银失去电子变成银离子,理论上溶液的物质的量浓度不变,pH保持不变,对;C、装置甲中开始的反应为:2KCl+2H2O2KOH+H2↑+Cl2↑,故要使溶液恢复可通入适最HCl气体即可,对;D、由装置甲发生的反应可得两电极产生的气体体积相等,所以产生氢气为2.24 L,转移电子0.2 mol,则铜电极上生成Ag0.2 mol,质量为21.6 g,错。

练习册系列答案
相关题目
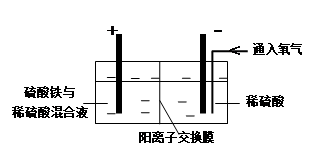
 R2Cu(有机相)+ 2H+(水相)
R2Cu(有机相)+ 2H+(水相)