题目内容
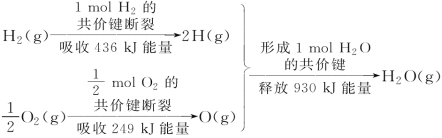
【题目】依据如图判断,下列说法正确的是( )
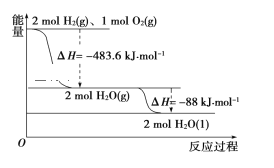
A. 氢气的燃烧热ΔH=-241.8 kJ·mol-1
B. 2 mol H2(g)与1mol O2(g)所具有的总能量比2 mol H2O(g)所具有的总能量低
C. 液态水分解的热化学方程式为2H2O(l)=2H2(g)+O2(g) ΔH=+571.6 kJ·mol-1
D. H2O(g)生成H2O(l)时,断键吸收的能量小于成键放出的能量
【答案】C
【解析】
A.氢气的燃烧热是指1mol氢气完全燃烧生成液态水放出的热量,故氢气的燃烧热为(483.6+88)/2=285.8 kJ·mol-1, A错误;
B. 2 mol H2(g)与1 mol O2(g)反应生成2 mol H2O(g),放出热量483.6 kJ,所以2 mol H2(g)与1 mol O2(g)所具有的总能量比2 mol H2O(g)所具有的总能量高,B错误;
C.液态水分解的热化学方程式为:2H2O(l)===2H2(g)+O2(g),ΔH=+(483.6+88)=+571.6 kJ·mol-1,C正确;
D.H2O(g)生成H2O(l)时,为物理变化,不存在化学键的断裂和生成,D错误;
正确选项C。

练习册系列答案
相关题目