题目内容
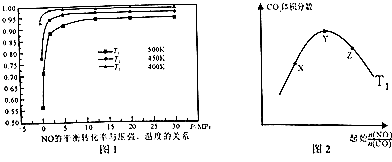
【题目】根据下图所示的信息,判断下列叙述不正确的是
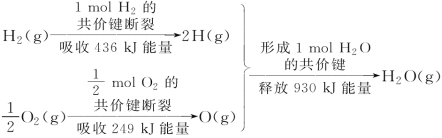
A.1 mol H2的共价键形成放出436 kJ能量
B.氢气跟氧气反应生成水的同时吸收能量
C.1 mol H2(g)跟![]() mol O2(g)反应生成1 mol H2O(g)释放能量245 kJ
mol O2(g)反应生成1 mol H2O(g)释放能量245 kJ
D.1 mol H2(g)与![]() mol O2(g)的总能量大于1 mol H2O(g)的能量
mol O2(g)的总能量大于1 mol H2O(g)的能量
【答案】B
【解析】
试题分析:A.对同一个化学键来说,断裂时吸收的能量与形成时放出的能量相等,A项正确;B.H2在O2中燃烧为放热反应,B项错误;C.ΔQ=Q(吸)-Q(放)=(436 kJ+249 kJ)-930 kJ=-245 kJ,说明该反应中释放出245 kJ能量,C项正确;D.放热反应的反应物总能量大于生成物总能量,D项正确;答案选B。

练习册系列答案
相关题目