题目内容
【题目】氮的固定是几百年来科学家一直研究的课题。
(1)下表列举了不同温度下大气固氮和工业固氮的部分K值。
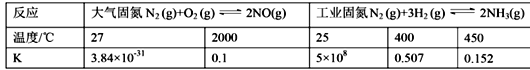
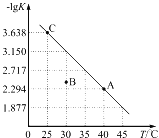
①分析数据可知:大气固氮反应属于 _______(填“吸热”或“放热”)反应。
②从平衡视角考虑,工业固氮应该选择常温条件,但实际工业生产却选择500℃左右的高温,解释其原因 _____________________________________________。
③在一定的温度下,把2体积N2和6体积H2分别通入一个带活塞的体积可变的容器中,活塞的一端与大气相通容器中发生如下反应:N2(g)+3H2(g)![]() 2NH3(g) △H<0。反应达到平衡后,测得混合气体为7体积。达到平衡时N2的转化率_______________________。
2NH3(g) △H<0。反应达到平衡后,测得混合气体为7体积。达到平衡时N2的转化率_______________________。
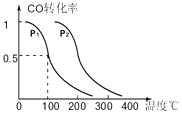
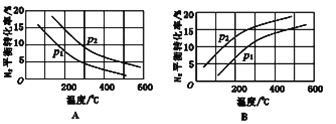
(2)工业固氮反应中,在其他条件相同时,分别测定N2的平衡转化率在不同压强(P1、P2)下随温度变化的曲线,下图所示的图示中,正确的是_______(填“A”或“B”);比较p1、p2的大小关系: p1_______________p2(填“>”或“<”)。
【答案】 吸热 从反应速率角度考虑,高温更好,从催化剂活性等综合因素考虑选择500℃左右合适 25% A <
【解析】(1)①由表格数据可知,大气固氮温度越高,K越大,说明升高温度,平衡正移,则正反应方向为吸热反应,
故答案为:吸热;
②由表格数据可知,合成氨反应温度越高,K越小,说明合成氨反应为放热反应,温度高转化率会降低,所以从平衡的视角来看,工业固氮应该选择常温条件;但是常温下,合成氨反应速率小,效率低,而且在500℃左右催化剂活性最高,所以从催化剂活性、化学反应速率等综合因素考虑选择500℃左右合适。
故答案为:从反应速率角度考虑,高温更好,从催化剂活性等综合因素考虑选择500℃左右合适。
③恒温恒压下,气体体积之比等于物质的量之比。平衡之后,气体由8体积变为7体积,则体积变化量为1。
根据方程式可知: N2(g)+3H2(g)2NH3(g)~△v
1 2
0.5 1
所以,氮气反应了0.5体积,转化率为: ![]()
故答案为:25%
(2)合成氨反应为放热反应,升高温度,转化率减小,所以图A正确,B错误;该反应正方向为体积减小的方向,增大压强平衡正向移动,转化率增大,p2的转化率大,则p2大,p2>p1。
故答案为:A;p2>p1;