题目内容
下图中每条折线表示周期表ⅣA~ⅦA中的某一族元素氢化物的沸点变化,每个小黑点代表一种氢化物,其中a点代表的是( )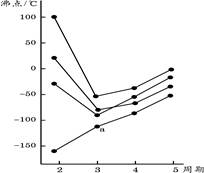
| A.H2S | B.HCl | C.PH3 | D.SiH4 |
D
解析试题分析:在ⅣA~ⅦA中的氢化物里,NH3、H2O、HF因存在氢键,故沸点高于同主族相邻元素氢化物的沸点,只有ⅣA族元素氢化物不存在反常现象,故a点代表的应是SiH4,D项正确。
考点:本题考查氢键的存以及对物质性质的影响。

练习册系列答案
相关题目
一种新催化剂,能在室温下催化空气氧化甲醛:HCHO+O2 CO2+H2O,该反应
CO2+H2O,该反应
| A.反应物和生成物中都含极性分子和非极性分子 |
| B.生成1.8gH2O消耗2.24L O2 |
| C.反应时有极性键和非极性键的断裂和它们的生成 |
| D.为吸热反应 |
下列各组物质的晶体中,化学键类型相同、晶体类型也相同的是
| A.SO2和SiO2 | B.CCl4和KCl | C.NaCl和HCl | D.CO2和H2O |
2004年7月德俄两国化学家共同宣布,在高压下氮气会发生聚合得到高聚氮,这种高聚氮的N-N键的键能为160kJ/mol(N2的键能为942kJ/mol),晶体片段结构如图所示。又发现从N2可制取出N5、N3。含N5+离子的化合物及N60、N5极不稳定。则下列说法错误的是:
| A.该晶体中含有非极性共价键 |
| B.含N5+离子的化合物中既有离子键又有共价键 |
| C.高聚氮与N2、N3、N5、N5+、N60互为同素异形体 |
| D.这种固体的可能潜在应用是烈性炸药或高能材料 |
三硫化磷(P4S3)是黄绿色针状晶体,易燃、有毒,分子结构之一如下图所示,已知其燃烧热△H=-3677kJ/mol(P被氧化为P4O10),下列有关P4S3的说法中不正确的是
| A.分子中每个原子最外层均达到8电子稳定结构 |
| B.P4S3中硫元素为-2价磷元素为+3价 |
| C.热化学方程式为P4S3( s)+8O2(g) =P4O10(s )+3SO2(g)△H=-3677kJ/mol |
| D.一个P4S3分子中含有三个非极性共价键 |
下列说法中错误的是( )
| A.当中心原子的配位数为6时,配合单元常呈八面体空间结构 |
| B.[Ag(NH3)2]+中Ag+空的5S轨道和5P轨道以sp杂化成键 |
| C.配位数为4的配合物均为正四面体结构 |
| D.已知[Cu(NH3)2]2+的中心原子采用sp杂化,则它们的空间构型为直线型 |
对σ键和π键的认识不正确的是
| A.σ键和π键不属于共价键,是另一种化学键 |
| B.s-sσ键与s-pσ键的电子云均为轴对称图形 |
| C.分子中含有共价键,则至少含有一个σ键 |
| D.含有π键的化合物与只含σ键的化合物的化学性质不同 |
下列物质中,既有离子键,又有共价键的是
| A.HCl | B.KOH | C.CaCl2 | D.CH3COOH |
化学键是相邻原子间强烈的相互作用,主要有离子键、共价键等。有关它们叙述正确的是
| A.非金属元素组成的化合物中只含共价键 |
| B.不同元素的原子构成的分子只含极性共价键 |
| C.熔融状态下能够导电的化合物中存在离子键 |
| D.单质分子中均存在化学键 |