题目内容
有KCl和KBr的混合物3.87 g溶于水配成溶液,向溶液中加入足量的AgNO3溶液,得到6.63 g沉淀,则混合物中含K元素的质量分数约为( )?
| A.50% | B.30% |
| C.60% | D.40% |
D?
初步审题,感觉是一道混合物的计算。仔细分析,可以发现KCl和KBr的混合物溶于水配成溶液,向溶液中加入足量的AgNO3溶液,得到沉淀,沉淀是AgCl和AgBr的混合物。3.87 g变成6.63 g,是K元素和Ag元素的质?量差?。?
6.63 g - 3.87 g = 2.76 g?
K ~ Ag Δm??
39 108 69?
m(K) 2.76 g
m(K)=39×2.76 g/108="1.56" g,混合物中含K元素的质量分数: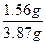 ×100%=40%。
×100%=40%。
6.63 g - 3.87 g = 2.76 g?
K ~ Ag Δm??
39 108 69?
m(K) 2.76 g
m(K)=39×2.76 g/108="1.56" g,混合物中含K元素的质量分数:
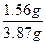 ×100%=40%。
×100%=40%。
练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目
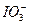 ;
;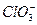 >Cl2>
>Cl2>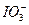 >I2。现将饱和氯水逐滴滴入KI淀粉溶液中至过量。
>I2。现将饱和氯水逐滴滴入KI淀粉溶液中至过量。 SiC+2CO↑。在这个氧化还原反应中,氧化剂和还原剂的物质的量之比是( )
SiC+2CO↑。在这个氧化还原反应中,氧化剂和还原剂的物质的量之比是( )