题目内容
下列表示电子式的形成过程正确的是:
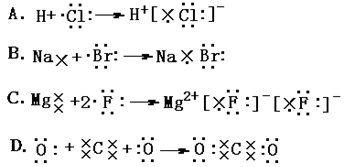
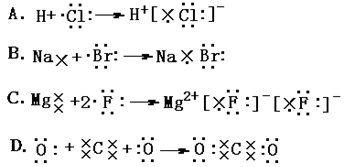
D
氯化氢是由极性键形成的共价化合物,形成过程是 。溴化钠是离子化合物,形成过程表示为
。溴化钠是离子化合物,形成过程表示为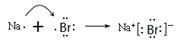 。氟化镁也是离子化合物,形成过程可表示为
。氟化镁也是离子化合物,形成过程可表示为
 ,所以正确的答案是D。
,所以正确的答案是D。
 。溴化钠是离子化合物,形成过程表示为
。溴化钠是离子化合物,形成过程表示为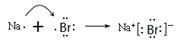 。氟化镁也是离子化合物,形成过程可表示为
。氟化镁也是离子化合物,形成过程可表示为 ,所以正确的答案是D。
,所以正确的答案是D。
练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案
相关题目
题目内容
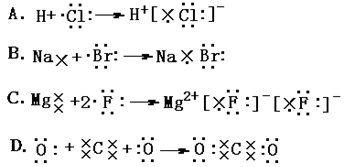
 。溴化钠是离子化合物,形成过程表示为
。溴化钠是离子化合物,形成过程表示为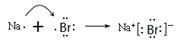 。氟化镁也是离子化合物,形成过程可表示为
。氟化镁也是离子化合物,形成过程可表示为 ,所以正确的答案是D。
,所以正确的答案是D。
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案