题目内容
下列叙述中正确的是
- A.加热蒸干灼烧FeCl3溶液,最后所得固体为Fe(OH)3
- B.将pH=4的醋酸溶液稀释后,溶液中所有离子浓度都降低
- C.pH相同,体积相同的醋酸溶液和稀硫酸分别与足量锌充分反应,产生氢气的量相同
- D.若弱酸HA的酸性强于弱酸HB,则同浓度钠盐溶液的碱性:NaA<NaB
D
试题分析:A加热FeCl3溶液,由于氯化铁水解产生氢氧化铁和氯化氢,氯化氢又挥发性,会随着水分的蒸发而挥发掉,蒸干得到固体为Fe(OH)3灼烧,Fe(OH)3分解产生氧化铁和水最后所得固体为Fe2O3。错误。B在醋酸溶液稀释的过程中氢离子、醋酸根离子的浓度降低,但由于溶液中存在水的电离平衡。在溶液中氢离子和氢氧根离子的浓度的乘积是个常数。所以在醋酸溶液稀释的过程中氢离子浓度降低,氢氧根离子的浓度增大。错误。C.pH相同,体积相同的醋酸溶液和稀硫酸中氢离子的物质的量相等。由于硫酸是强酸,全部电离;醋酸是弱酸,部分电离。所以最终产生氢离子的物质的量是醋酸大于硫酸。分别与足量锌充分反应,产生氢气的量醋酸的也就大于硫酸的。错误。D.盐的水解规律是:谁弱谁水解,谁强显谁性,越弱越水解,都强不水解。由于弱酸HA的酸性强于弱酸HB,则同浓度钠盐溶液的碱性:NaA<NaB。正确。
考点:考查盐的水解规律的应用及溶液稀释问题的知识。
试题分析:A加热FeCl3溶液,由于氯化铁水解产生氢氧化铁和氯化氢,氯化氢又挥发性,会随着水分的蒸发而挥发掉,蒸干得到固体为Fe(OH)3灼烧,Fe(OH)3分解产生氧化铁和水最后所得固体为Fe2O3。错误。B在醋酸溶液稀释的过程中氢离子、醋酸根离子的浓度降低,但由于溶液中存在水的电离平衡。在溶液中氢离子和氢氧根离子的浓度的乘积是个常数。所以在醋酸溶液稀释的过程中氢离子浓度降低,氢氧根离子的浓度增大。错误。C.pH相同,体积相同的醋酸溶液和稀硫酸中氢离子的物质的量相等。由于硫酸是强酸,全部电离;醋酸是弱酸,部分电离。所以最终产生氢离子的物质的量是醋酸大于硫酸。分别与足量锌充分反应,产生氢气的量醋酸的也就大于硫酸的。错误。D.盐的水解规律是:谁弱谁水解,谁强显谁性,越弱越水解,都强不水解。由于弱酸HA的酸性强于弱酸HB,则同浓度钠盐溶液的碱性:NaA<NaB。正确。
考点:考查盐的水解规律的应用及溶液稀释问题的知识。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
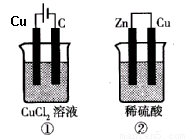
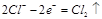 ②中负极
②中负极