题目内容
(1)计算HNO3被还原的物质的量;
(2)计算合金中银的质量分数。
(1)0.30 mol (2)0.36
题设条件下,发生的反应有:
Cu+4HNO3(浓)====Cu(NO3)2+2NO2↑+2H2O
3Cu+8HNO3(稀)====3Cu(NO3)2+2NO↑+4H2O
Ag+2HNO3(浓)====AgNO3+NO2↑+H2O
3Ag+4HNO3(稀)====3AgNO3+NO↑+2H2O
(1)n(被还原HNO3)=n(NO2)+n(NO)= ="0.300" mol
="0.300" mol
(2)设合金中Cu和Ag的物质的量分别为x、y。则:
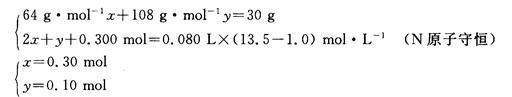
w(Ag)=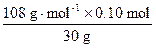 =0.36
=0.36
Cu+4HNO3(浓)====Cu(NO3)2+2NO2↑+2H2O
3Cu+8HNO3(稀)====3Cu(NO3)2+2NO↑+4H2O
Ag+2HNO3(浓)====AgNO3+NO2↑+H2O
3Ag+4HNO3(稀)====3AgNO3+NO↑+2H2O
(1)n(被还原HNO3)=n(NO2)+n(NO)=
 ="0.300" mol
="0.300" mol(2)设合金中Cu和Ag的物质的量分别为x、y。则:
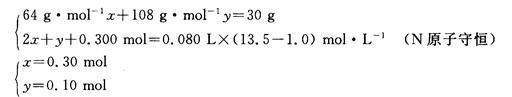
w(Ag)=
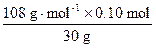 =0.36
=0.36
练习册系列答案
相关题目
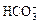 离子数为6.02×1023[
离子数为6.02×1023[ Cu+H2O
Cu+H2O