题目内容
【题目】下列有关实验现象的记录不正确的是( )
A. 钠可以在氯气中燃烧,产生白色的烟,火焰黄色
B. 红热的铁丝可以在氯气中燃烧,产生绿色的烟
C. 为了防止储存液氯的钢桶被腐蚀,装氯前必须彻底干燥
D. 盛满 CO2 气体的试管倒插入氢氧化钠溶液中,一段时间后,试管内充满液体
【答案】B
【解析】A. 钠可以在氯气中燃烧,产生白色的烟,火焰黄色,A正确;B. 红热的铁丝可以在氯气中燃烧,产生棕黄色的烟,B错误;因氯气与水反应生成盐酸,盐酸与铁反应,故装氯前必须彻底干燥钢桶,为了防止钢桶被腐蚀,C正确;二氧化碳易被氢氧化钠溶液吸收,压强减小,液面上升,D正确。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】甲醇是重要的化工原料,又可做为燃料.利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
ⅠCO(g)+2H2(g)CH3OH(g)△H1
ⅡCO2(g)+3H2(g)CH3OH(g)+H2O(g)△H2=﹣58kJ/mol
ⅢCO2(g)+H2(g)CO(g)+H2O(g)△H3
回答下列问题:
(1)物质的标准生成热是常用的化学热力学数据,可以用来计算化学反应热.即化学反应热:△H=生成物标准生成热综合﹣反应物标准生成热总和.
已知四种物质的标准生成热如表:
物质 | CO | CO2 | H2 | CH3OH(g) |
标准生成热(kJ/mol) | ﹣110.52 | ﹣393.51 | 0 | ﹣201.25 |
A.计算△H1=kJ/mol B.△H30(填=、<、>)
(2)由甲醇在一定条件下制备甲醚.一定温度下,在三个体积均为1.0L的恒容密闭容器中发生反应:2CH3OH(g)CH3OCH3(g)+H2O(g).实验数据见表:
容器编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |||
CH3OH(g) | CH3OCH3(g) | H2O(g) | CH3OCH3(g) | H2O(g) | ||
a | 387 | 0.20 | 0 | 0 | 0.080 | 0.080 |
b | 387 | 0.40 | 0 | 0 | ||
c | 207 | 0.20 | 0 | 0 | 0.090 | 0.090 |
下列说法正确的是
A.该反应的正反应为放热反应
B.达到平衡时,容器a中的CH3OH体积分数比容器b中的小
C.容器a中反应到达平衡所需时间比容器c中的长
D.若起始时向容器a中充入CH3OH 0.15mol、CH3OCH3 0.15mol和H2O 0.10mol,则反应将向正反应方向进行
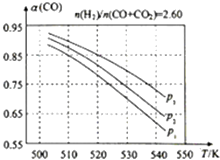
(3)合成气的组成 ![]() =2.60时,体系中的CO平衡转化率(α)与温度和压强的关系如图所示.
=2.60时,体系中的CO平衡转化率(α)与温度和压强的关系如图所示.
①α(CO)值随温度升高而(填“增大”或“减小”),其原因是 .
②图中P1、P2、P3的大小关系为 , 其判断理由是 .
(4)甲醇可以制成燃料电池,与合成气制成燃料电池相比优点是:;若以硫酸作为电解质其负极反应为: .