题目内容
已知电极材料:铁、铜、银、石墨、锌、铝;电解质溶液:CuCl2溶液、Fe2(SO4)3溶液、盐酸.按要求回答下列问题:
(1)电工操作上规定:不能把铜导线和铝导线连接在一起使用.请说明原因
(2)若电极材料选铜和石墨,电解质溶液选硫酸铁溶液,外加导线,能否构成原电池
(3)设计一种以铁和硫酸反应为原理的原电池,要求画出装置图:(需标明电极材料及电池的正负.)
(1)电工操作上规定:不能把铜导线和铝导线连接在一起使用.请说明原因
二者连接在一起时,
二者连接在一起时,
.(2)若电极材料选铜和石墨,电解质溶液选硫酸铁溶液,外加导线,能否构成原电池
能
能
,若能,请写出电极反应式,负极Cu-2e-→Cu2+
Cu-2e-→Cu2+
,正极2Fe3++2e-→2Fe2+
2Fe3++2e-→2Fe2+
.(若不能,后两空不填)(3)设计一种以铁和硫酸反应为原理的原电池,要求画出装置图:(需标明电极材料及电池的正负.)
分析:(1)根据原电池的构成条件和造成的危害角度来回答;
(2)所有自发的氧化还原反应均可以设计成原电池,负极发生失电子的氧化反应,正极发生还原反应;
(3)铁和硫酸反应时,是电子的是金属铁,得电子的是氢离子,据此来选择电极材料和电解质.
(2)所有自发的氧化还原反应均可以设计成原电池,负极发生失电子的氧化反应,正极发生还原反应;
(3)铁和硫酸反应时,是电子的是金属铁,得电子的是氢离子,据此来选择电极材料和电解质.
解答:解:(1)把铜导线和铝导线连接在一起使用时,接头处在潮湿的空气中形成原电池而腐蚀,所以不能把铜导线和铝导线连接在一起使用,故答案为:二者连接在一起时,接头处在潮湿的空气中形成原电池而腐蚀;
(2)金属铜和硫酸铁之间能发生自发的氧化还原反应,可以设计成原电池,金属铜在负极上失电子,发生氧化反应,Cu-2e-→Cu2+,在正极上是三价铁得到电子,发生还原反应,2Fe3++2e-→2Fe2+,
故答案为:能,Cu-2e-→Cu2+,2Fe3++2e-→2Fe2+;
(3)铁和硫酸反应中,失电子的是金属铁,金属铁一定做负极,正极材料应该是活泼性比金属铁差的一种光导体,电解质为硫酸,即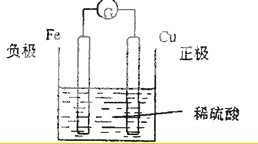 ,故答案为:
,故答案为: .
.
(2)金属铜和硫酸铁之间能发生自发的氧化还原反应,可以设计成原电池,金属铜在负极上失电子,发生氧化反应,Cu-2e-→Cu2+,在正极上是三价铁得到电子,发生还原反应,2Fe3++2e-→2Fe2+,
故答案为:能,Cu-2e-→Cu2+,2Fe3++2e-→2Fe2+;
(3)铁和硫酸反应中,失电子的是金属铁,金属铁一定做负极,正极材料应该是活泼性比金属铁差的一种光导体,电解质为硫酸,即
 ,故答案为:
,故答案为: .
.点评:本题考查学生原电池的工作原理以及设计成原电池的化学反应需要是自发的氧化还原反应这一知识,可以根据所学知识进行回答,难度不大.

练习册系列答案
 53天天练系列答案
53天天练系列答案
相关题目
 已知电极材料:铁、铜、银、石墨、锌、铝;
已知电极材料:铁、铜、银、石墨、锌、铝;