��Ŀ����
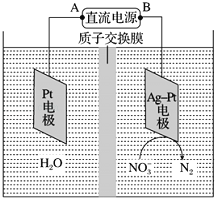
����Ŀ���ֱ���ͼ�ס�����ʾװ�ý���ʵ�飬ͼ�������ձ������ҺΪͬŨ�ȵ�ϡ���ᣬ����AΪ����������ش���������:

(1)���������У���ȷ����_______(����ĸ).
A ����пƬ�Ǹ���������ͭƬ������ B ���ձ���ͭƬ����������ݲ���
C ���ձ�����ҺpH������ D �������ݵ��ٶȼ��б�������
E �ҵ����·�е�������Zn��Cu F ����Һ��SO42-��ͭƬ�����ƶ�
(2)�仯����������ת������Ҫ��ʽ:��Ϊ_________����Ϊ________��
(3)����ʵ���У�ijͬѧ���ֲ�����ͭƬ�������ݲ�����������пƬ��Ҳ���������壬����ԭ�������____��
(4)����ʵ���У���������ỻ������ͭ��Һ����д��ͭ�缫�ĵ缫��Ӧ����ʽ:__________������·��ת��0.25mo1����ʱ�����ĸ������ϵ�����Ϊ________��
���𰸡�CD ��ѧ��ת��Ϊ���� ��ѧ��ת��Ϊ���� пƬ��������пƬ�Ͼ��γ���ԭ��� Cu2����2e��===Cu 8.125g
��������
��װ��ͭ��пû�й��ɱպϵ�·������ԭ��أ�п�����ᷴӦ�ų���������װ�ù���ԭ��أ�п�Ļ����Դ���ͭ��п�Ǹ�����пʧ���ӷ���������Ӧ��ͭ��������ͭ�缫�������ӵõ��ӷ�����ԭ��Ӧ����������
(1) A. ��װ��ͭ��пû�й��ɱպϵ�·������ԭ��أ���A����
B.���ձ�û�й���ԭ��أ���ͭ�������Ӧ�����Լ��ձ���ͭƬ����û�����ݲ�������B����
C.���ձ��ж��������ų������ձ�����ҺpH������C��ȷ��
D.�ҹ���ԭ��ء���û�й���ԭ��أ����Բ������ݵ��ٶȼ��б�����������D��ȷ��
E.��������������������ԭ��أ�ͭ�����������·�е�������Cu��Zn����E����
F.ԭ���������������������Һ��SO42-��пƬ�����ƶ�����F����
(2)��û�й���ԭ��أ���ѧ��ת��Ϊ���ܣ���Ϊԭ��أ���ѧ��ת��Ϊ���ܡ�
(3) ��пƬ��������пƬ��п�������γ�ԭ��أ���ʱ������ͭƬ�������ݲ�����������пƬ��Ҳ���������塣
(4)����ʵ���У���������ỻ������ͭ��Һ��ͭ�����������õ�������ͭ��ͭ�缫�ĵ缫��Ӧ����ʽCu2����2e��===Cu��������Ӧʽ��Zn-2 e��=Zn2��������·��ת��0.25mo1����ʱ�����ĸ������ϵ�����Ϊ![]() 8.125g��
8.125g��