题目内容
运用化学反应原理研究碳、氮等元素的单质及其化合物的反应有重要意义.
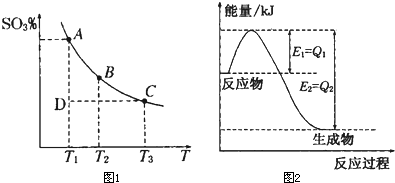
(1)如图1表示金刚石、石墨在相关反应过程中的能量变化关系.写出石墨转化为金刚石的热化学方程式 .

(2)CO与H2可在一定条件下反应生成燃料甲醇:CO(g)+2H2(g)?CH3OH(g)△H<0
将2molCO和4molH2置于一体积不变的1L密闭容器中,测定不同条件、不同时间段内CO的转化率,得到下表数据.
则温度为T1时该反应的平衡常数为 .
a1、a2、80%三者的大小关系为 .(选填“>”“<”“=”无法比较”)根据温度为T1时的数据作出的下列判断中正确的是 .
A.反应在2小时的时候混合气体的密度和相对分子质量均比l小时的大B.反应在3小时的时候,v正(H2)=2v逆(CH30H)
C.若其他条件不变,再充入6molH2,则最多可得到64g CH3OH
D.其他条件不变,若最初加入的H2为2.4mol,则达平衡时CO的转化率为50%
(3)工业中常用以下反应合成氨:N2+3H2?2NH3△H<0.在三个不同条件的密闭容 器中,分别加入浓度均为c(N2)=0.10mol/L,c(H2)=0.30mol/L进行反应时,N2的浓度随时间的变化如图2中的①、②、③曲线所示.
计算③中产物NH3在0-10min的平均反应速率 ②相对于①条件不同,指出②的条件是 ,理由是 .
(1)如图1表示金刚石、石墨在相关反应过程中的能量变化关系.写出石墨转化为金刚石的热化学方程式

(2)CO与H2可在一定条件下反应生成燃料甲醇:CO(g)+2H2(g)?CH3OH(g)△H<0
将2molCO和4molH2置于一体积不变的1L密闭容器中,测定不同条件、不同时间段内CO的转化率,得到下表数据.
| 时间 \CO转化率 \温度 |
1小时 | 2小时 | 3小时 | 4小时 |
| T1 | 30% | 50% | 80% | 80% |
| T2 | 35% | 60% | a1 | a2 |
a1、a2、80%三者的大小关系为
A.反应在2小时的时候混合气体的密度和相对分子质量均比l小时的大B.反应在3小时的时候,v正(H2)=2v逆(CH30H)
C.若其他条件不变,再充入6molH2,则最多可得到64g CH3OH
D.其他条件不变,若最初加入的H2为2.4mol,则达平衡时CO的转化率为50%
(3)工业中常用以下反应合成氨:N2+3H2?2NH3△H<0.在三个不同条件的密闭容 器中,分别加入浓度均为c(N2)=0.10mol/L,c(H2)=0.30mol/L进行反应时,N2的浓度随时间的变化如图2中的①、②、③曲线所示.
计算③中产物NH3在0-10min的平均反应速率
分析:(1)依据物质能量越高,越活泼分析判断,依据图象能量变化写出石墨转化为金刚石的热化学方程式,反应是吸热反应;
(2)化学平衡常数,是指在一定温度下,可逆反应达到平衡时各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,据此书写;根据T1和T2同时间段内CO的转化率可知T2反应温度高;温度为T1时A.混合气体的密度不变;B.反应在3小时的时候,已达平衡;C.该反应为可逆反应,CO不可能全部转化;D.根据同一温度平衡常数不变,进行解答;
(3)根据化学反应速率的计算公式进行解答;②到达平衡的时间比①短,到达平衡时N2的浓度与①相同,化学平衡不移动;
(2)化学平衡常数,是指在一定温度下,可逆反应达到平衡时各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,据此书写;根据T1和T2同时间段内CO的转化率可知T2反应温度高;温度为T1时A.混合气体的密度不变;B.反应在3小时的时候,已达平衡;C.该反应为可逆反应,CO不可能全部转化;D.根据同一温度平衡常数不变,进行解答;
(3)根据化学反应速率的计算公式进行解答;②到达平衡的时间比①短,到达平衡时N2的浓度与①相同,化学平衡不移动;
解答:解:(1)根据图象分析金刚石能量高于石墨,能量越低越稳定,所以说明石墨稳定,根据图象石墨转化为金刚石需要吸收热量=395.4KJ-393.5KJ=1.9KJ;所以反应的热化学方程式为C(石墨,s)═C(金刚石,s)△H=+1.9 kJ?mol-1
故答案为:C(石墨,s)═C(金刚石,s)△H=+1.9 kJ?mol-1;
(2)2molCO和4molH2置于一体积不变的1L密闭容器中,温度为T1时CO的转化率为80%,转化1.6mol/L,
CO(g)+2H2(g)?CH3OH(g)△H<0
开始2mol/L 4mol/L 0
转化1.6mol/L 3.2mol/L 1.6mol/L
平衡0.4mol/L 0.8mol/L 1.6mol/L
则化学平衡常数K=
=6.25L2/mol2;
根据T1和T2同时间段内CO的转化率可知T2反应温度高,CO(g)+2H2(g)?CH3OH(g)△H<0,正反应为放热反应,所以T2相当于T1达到平衡时加热,平衡向逆反应方向移动,达平衡时,CO的转化率较T1时低,a1=a2、表示已达平衡,所以a1═a2<80%;
A.该反应体积固定,1L密闭容器,反应 CO(g)+2H2(g)?CH3OH(g)反应物和产物都是气体,所以在2小时的时候混合气体的密度和l小时的一样大,由于正反应是物质的量减少的反应,所以反应在2小时的时候混合气体的相对分子质量均比l小时的大,故A错误;
B.反应在3小时的时候,CO的转化率为80%,已达平衡,v正(H2)说明反应正向进行,v逆(CH30H)说明反应逆向进行,v正(H2)=2v逆(CH30H),表示该反应达平衡,故B正确;
C.该反应为可逆反应,若其他条件不变,再充入6molH2,2molCO无法全部转化,所以得到 CH3OH小于64g,故C错误;
D.其他条件不变,若最初加入的H2为2.4mol,根据温度不变,平衡常数不变,设达平衡时CO的转化率为X,
CO(g)+2H2(g)?CH3OH(g)△H<0
开始 2mol/L 2.4mol/L 0
转化 2Xmol/L 4Xmol/L 2Xmol/L
平衡 (2-2X)mol/L (2.4-4X)mol/L 2Xmol/L
=6.25L2/mol2,X=0.5,故D正确;
故答案为:6.25L2/mol2;a1═a2<80%;BD;
(3)由图2可知,反应中N2在0-10min的浓度变化为0.1mol/L-0.08mol/L=0.02mol/L,10min时达到平衡,根据N2+3H2?2NH3可知:氨气的浓度变化为:0.04mol/L;则用NH3表示的化学反应速率为V=
=
=0.0040 mol?L-1?min-1;
②到达平衡的时间比①短,到达平衡时N2的浓度与①相同,化学平衡不移动,因为加入催化剂能缩短达到平衡的时间,但化学平衡不移动,故②与①相比加了催化剂,
故答案为:0.0040 mol?L-1?min-1;加入催化剂;装置②到达平衡的时间缩短,且②中到达平衡时氮气浓度与①相同;
故答案为:C(石墨,s)═C(金刚石,s)△H=+1.9 kJ?mol-1;
(2)2molCO和4molH2置于一体积不变的1L密闭容器中,温度为T1时CO的转化率为80%,转化1.6mol/L,
CO(g)+2H2(g)?CH3OH(g)△H<0
开始2mol/L 4mol/L 0
转化1.6mol/L 3.2mol/L 1.6mol/L
平衡0.4mol/L 0.8mol/L 1.6mol/L
则化学平衡常数K=
| 1.6mol/L |
| (0.8mol/L)2×0.4mol/L |
根据T1和T2同时间段内CO的转化率可知T2反应温度高,CO(g)+2H2(g)?CH3OH(g)△H<0,正反应为放热反应,所以T2相当于T1达到平衡时加热,平衡向逆反应方向移动,达平衡时,CO的转化率较T1时低,a1=a2、表示已达平衡,所以a1═a2<80%;
A.该反应体积固定,1L密闭容器,反应 CO(g)+2H2(g)?CH3OH(g)反应物和产物都是气体,所以在2小时的时候混合气体的密度和l小时的一样大,由于正反应是物质的量减少的反应,所以反应在2小时的时候混合气体的相对分子质量均比l小时的大,故A错误;
B.反应在3小时的时候,CO的转化率为80%,已达平衡,v正(H2)说明反应正向进行,v逆(CH30H)说明反应逆向进行,v正(H2)=2v逆(CH30H),表示该反应达平衡,故B正确;
C.该反应为可逆反应,若其他条件不变,再充入6molH2,2molCO无法全部转化,所以得到 CH3OH小于64g,故C错误;
D.其他条件不变,若最初加入的H2为2.4mol,根据温度不变,平衡常数不变,设达平衡时CO的转化率为X,
CO(g)+2H2(g)?CH3OH(g)△H<0
开始 2mol/L 2.4mol/L 0
转化 2Xmol/L 4Xmol/L 2Xmol/L
平衡 (2-2X)mol/L (2.4-4X)mol/L 2Xmol/L
| 2Xmol/L |
| [(2-2X)mol/L]×[(2.4-4X)mol/L]2 |
故答案为:6.25L2/mol2;a1═a2<80%;BD;
(3)由图2可知,反应中N2在0-10min的浓度变化为0.1mol/L-0.08mol/L=0.02mol/L,10min时达到平衡,根据N2+3H2?2NH3可知:氨气的浓度变化为:0.04mol/L;则用NH3表示的化学反应速率为V=
| △C(NH3) |
| t |
| 0.04mol/L |
| 10min |
②到达平衡的时间比①短,到达平衡时N2的浓度与①相同,化学平衡不移动,因为加入催化剂能缩短达到平衡的时间,但化学平衡不移动,故②与①相比加了催化剂,
故答案为:0.0040 mol?L-1?min-1;加入催化剂;装置②到达平衡的时间缩短,且②中到达平衡时氮气浓度与①相同;
点评:本题主要以CO与H2在一定条件下反应生成燃料甲醇为载体,重点考查了化学平衡常数、影响因素及有关计算、平衡的判断等,注意计算平衡常数时表达式中的浓度为平衡浓度,不是任意时刻的浓度,题目难度较大.

练习册系列答案
相关题目
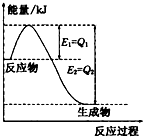 运用化学反应原理研究氮、氯、碘等单质及其化合物的反应有重要意义.
运用化学反应原理研究氮、氯、碘等单质及其化合物的反应有重要意义.