题目内容
食盐是日常生活的必需品,也是重要的化工原料。
(1)粗食盐常含有少里K+、Ca2+、Mg2+、Fe3+、SO42-等杂质离子,实验室提纯NaCl的流程如下:
提供的试剂:饱和Na2CO3溶液 饱和K2CO3溶液 NaOH溶液 BaCl2溶液 Ba(NO3)2溶液欲除去溶液I中的Ca2+、Mg2+、Fe3+、SO42-离子,选出a所代表的试剂,按滴加顺序依次为 ___(只填化学式)。
(2)用提纯的NaCl配制500mL 4.00 mol·L-1 NaCl溶液,所用仪器除药匙、玻璃棒外还有 (填仪器名称)。
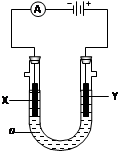
(3)电解饱和食盐水的装置如图所示,若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式为 。在X极附近观察到的实验现象是 。
②Y电极上的电极反应式为 。检验该电极反应产物的方法是 。
③若收集的H2为2 L ,则同样条件下收集的Cl2 (填“>”、“=” 或“<” 2 L,原因是 。
2 L,原因是 。
(1)粗食盐常含有少里K+、Ca2+、Mg2+、Fe3+、SO42-等杂质离子,实验室提纯NaCl的流程如下:
提供的试剂:饱和Na2CO3溶液 饱和K2CO3溶液 NaOH溶液 BaCl2溶液 Ba(NO3)2溶液欲除去溶液I中的Ca2+、Mg2+、Fe3+、SO42-离子,选出a所代表的试剂,按滴加顺序依次为 ___(只填化学式)。
(2)用提纯的NaCl配制500mL 4.00 mol·L-1 NaCl溶液,所用仪器除药匙、玻璃棒外还有 (填仪器名称)。
(3)电解饱和食盐水的装置如图所示,若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则

①电解池中X极上的电极反应式为 。在X极附近观察到的实验现象是 。
②Y电极上的电极反应式为 。检验该电极反应产物的方法是 。
③若收集的H2为2 L ,则同样条件下收集的Cl2 (填“>”、“=” 或“<”
 2 L,原因是 。
2 L,原因是 。(1)BaCl2、NaOH、Na2CO3(错选或多选本小题不得分。)NaOH溶液的加入顺序及是否答NaOH不影响得分
(2)天平、烧怀、500mL容量瓶、胶头滴管(3)①2H++2e-=H2↑ 放出气体,溶液变红
②2Cl—2e-=Cl2↑ 把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色。
③ < 电解生成的氯气与电解生成的NaOH发生了反应
(2)天平、烧怀、500mL容量瓶、胶头滴管(3)①2H++2e-=H2↑ 放出气体,溶液变红
②2Cl—2e-=Cl2↑ 把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色。
③ < 电解生成的氯气与电解生成的NaOH发生了反应
(1)考查物质的分离和提纯。除去Ca2+、Mg2+、Fe3+、SO42-离子的试剂分别是乙酸钠、氢氧化钠、氢氧化钠和氯化钡。由于过量的氯化钡需要碳酸钠来除去,所以碳酸钠必需放在氯化钡的后面,而氢氧化钠不受影响。
(2)考查一定物质的量浓度溶液的配制。根据实验原理可知,还缺少的仪器是天平(用来称量)、烧怀(用来溶解)、500mL容量瓶、胶头滴管(用来定容)。
(3)考查电化学的应用。
①根据装置图可知,X电极和电源的负极相连,作阴极,溶液中的氢离子放电,方程式是2H++2e-=H2↑;由于氢离子放电,破坏来阴极周围水的电离平衡,所以阴极周围溶液显碱性,则溶液呈红色。
②Y电极和电源的正极相连,作阳极,溶液中的氯离子放电,电极反应式是2Cl—2e-=Cl2↑;氯气具有氧化性,据此可以检验,即把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色。
③由于电解生成的氯气与电解生成的NaOH发生了反应,所以实际收集的氯气小于2L。
(2)考查一定物质的量浓度溶液的配制。根据实验原理可知,还缺少的仪器是天平(用来称量)、烧怀(用来溶解)、500mL容量瓶、胶头滴管(用来定容)。
(3)考查电化学的应用。
①根据装置图可知,X电极和电源的负极相连,作阴极,溶液中的氢离子放电,方程式是2H++2e-=H2↑;由于氢离子放电,破坏来阴极周围水的电离平衡,所以阴极周围溶液显碱性,则溶液呈红色。
②Y电极和电源的正极相连,作阳极,溶液中的氯离子放电,电极反应式是2Cl—2e-=Cl2↑;氯气具有氧化性,据此可以检验,即把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色。
③由于电解生成的氯气与电解生成的NaOH发生了反应,所以实际收集的氯气小于2L。

练习册系列答案
相关题目