题目内容
19.NA代表阿伏加德罗常数,下列说法正确的是( )| A. | 9g D2O中含有的电子数为5NA | |
| B. | 46g NO2和N2O4混合气体中含有原子数为3NA | |
| C. | 1mol C2H6分子中共价键总数为8NA | |
| D. | 7.1g C12与足量NaOH溶液反应转移的电子数为0.2NA |
分析 A.D2O的摩尔质量为20g/mol;
B.NO2和N2O4的最简式为NO2,根据最简式再计算出混合气体中含有的原子总数;
C.乙烷分子(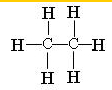 )中含有6个碳氢共价键和1个碳碳共价键,总共含有7个共价键,30个乙烷的物质的量为1mol,含有7mol共价键;
)中含有6个碳氢共价键和1个碳碳共价键,总共含有7个共价键,30个乙烷的物质的量为1mol,含有7mol共价键;
D.氯气与氢氧化钠发生歧化反应,氯从0价的单质氯变成-1价的NaCl中的氯,氯从0价的单质氯变成+1价的NaClO中的氯.
解答 解:A.9g D2O的物质的量为0.45mol,含有的电子数为4.5NA,故A错误;
B.46gNO2和N2O4混合气体中含有1mol最简式NO2,含有3mol原子,混合气体中含有原子总数为3NA,故B正确;
C.根据乙烷的结构式式 可知,1mol乙烷分子中含有6mol碳氢键和1mol碳碳键,总共含有7mol共价键,含有的共价键数为7NA,故C错误;
可知,1mol乙烷分子中含有6mol碳氢键和1mol碳碳键,总共含有7mol共价键,含有的共价键数为7NA,故C错误;
D.氯气与氢氧化钠反应:Cl2+2NaOH=NaCl+NaClO+H2O,1mol氯气完全反应,氯从0价的单质氯变成+1价的NaClO中的氯,失去1mol电子,氯从0价的单质氯变成-1价的NaCl中的氯,得到1mol电子,7.1gCl2为0.1mol,转移0.1NA电子,故D错误.
故选B.
点评 本题考查阿伏加德罗常数的相关计算,题目难度不大,注意物质的组成、结构、性质以及物质存在的外界条件和聚集状态等问题.

练习册系列答案
相关题目
9.下列实验操作不能达到预期目的是( )
| 实验目的 | 操作 | |
| A | 比较水和乙醇中羟基氢的活泼性 | 用金属钠分别与水和乙醇反应 |
| B | 证明HOCH2CHO中含有醛基 | 滴加酸性KMnO4溶液,看紫红色是否褪去 |
| C | 确定磷、砷两元素非金属性的强弱 | 测定同温同浓度的Na3PO4和Na3AsO4水溶液的pH |
| D | 除去苯中混有的苯酚 | 向混合液中加入NaOH溶液,充分反应后,分液 |
| A. | A | B. | B | C. | C | D. | D |
4.化学无处不在,下列与化学有关的说法不正确的是( )
| A. | 侯氏制碱法的工艺过程中应用了物质溶解度的差异 | |
| B. | 可用蘸浓硫酸的棉棒检验输送氨气的管道是否漏气 | |
| C. | 碘是人体必需微量元素,所以要适量吃富含碘酸根原子团的食物 | |
| D. | 黑火药由硫黄、硝石、木炭三种物质按一定比例混合制成 |
11.下列实验操作或装置正确的是( )
| A. | 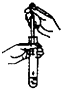 向试管中滴加液体 | B. | 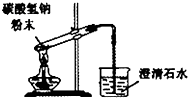 碳酸氢钠受热分解 | ||
| C. | 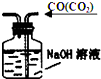 除去CO气体中的CO2气体 | D. | 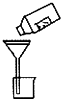 过滤 |
8.已知 W、X、Y、Z为短周期主族元素,W、Z同主族,X、Y、Z同周期,W的气态氢化物的稳定性大于Z的气态氢化物的稳定性,X、Y为金属元素,X的阳离子的氧化性小于Y的阳离子的氧化性.下列说法正确的是( )
| A. | X、Y、Z、W的原子半径依次减小 | |
| B. | W与X形成的化合物中只可能含有离子键 | |
| C. | 在工业上X、Y都可以直接用加热分解的方法冶炼 | |
| D. | 若W与Y的原子序数相差5,则二者形成的化合物的化学式一定为Y2W3 |
9.在下列反应中,硫元素表现出氧化性的是( )
| A. | 二氧化硫与氧气反应 | B. | 三氧化硫与水反应 | ||
| C. | 稀硫酸与镁反应 | D. | 浓硫酸与碳反应 |
 .
.
 .
.