题目内容
(8分)单质A、B、C在常温下均为气态,分别由甲、乙、丙三种短周期元素组成;已知丙元素的原子结构中次外层电子数比最外层电子数多1,化合物D在常温下呈液态,G是常见的金属单质,H是常见的蓝色沉淀,各物质间的转化关系如图所示(反应条件多数已略去):
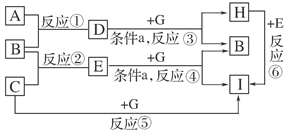
请回答:
(1)反应⑥的离子方程式是_______________________________________________。
(2)甲、乙两元素除形成化合物D外,还可形成一种含有4个原子核和18个电子的化合物,该化合物的电子式是________。
(3)在反应①中,已知1 g B完全燃烧生成液态D时,放出142.9 kJ的热量,则表示B的燃烧热的热化学方程式是_______________________________________________
________________________________________________________________________。
(4)反应①也可以设计成原电池装置进行,当用铂作电极,用KOH溶液作电解质溶液时,负极的电极反应式是________________________________________________________
________________________________________________________________________。
(5)反应③④在通常情况下不能自发进行,框图中的条件a是________,在使反应③④能够发生的装置中,有一个电极材料必须相同,写出该电极反应式________________________________________________________________________。

请回答:
(1)反应⑥的离子方程式是_______________________________________________。
(2)甲、乙两元素除形成化合物D外,还可形成一种含有4个原子核和18个电子的化合物,该化合物的电子式是________。
(3)在反应①中,已知1 g B完全燃烧生成液态D时,放出142.9 kJ的热量,则表示B的燃烧热的热化学方程式是_______________________________________________
________________________________________________________________________。
(4)反应①也可以设计成原电池装置进行,当用铂作电极,用KOH溶液作电解质溶液时,负极的电极反应式是________________________________________________________
________________________________________________________________________。
(5)反应③④在通常情况下不能自发进行,框图中的条件a是________,在使反应③④能够发生的装置中,有一个电极材料必须相同,写出该电极反应式________________________________________________________________________。
(1)Cu(OH)2+2H+===Cu2++2H2O
(2)H··············H
(3)H2(g)+O2(g)===H2O(l)
ΔH=-285.8 kJ·mol-1
(4)2H2-4e-+4OH-===4H2O
(5)通电(或电解) Cu-2e-===Cu2+
(2)H··············H
(3)H2(g)+O2(g)===H2O(l)
ΔH=-285.8 kJ·mol-1
(4)2H2-4e-+4OH-===4H2O
(5)通电(或电解) Cu-2e-===Cu2+
由题给信息知丙元素为Cl,H为Cu(OH)2,化合物D为H2O,则A为O2,B为H2,C为Cl2,G为Cu。

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
 :
:
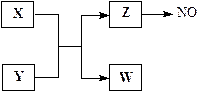
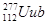 的一个原子经过6次衰变(每次衰变都放出一个相同的粒子)后,得到比较稳定的第100号元素镄(Fm)的含153个中子的原子。下列说法中正确的是( )
的一个原子经过6次衰变(每次衰变都放出一个相同的粒子)后,得到比较稳定的第100号元素镄(Fm)的含153个中子的原子。下列说法中正确的是( )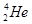
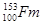 只是元素镄的一个原子,153不代表镄元素的相对原子质量
只是元素镄的一个原子,153不代表镄元素的相对原子质量
 种化学式 。
种化学式 。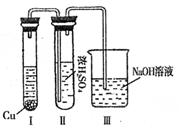
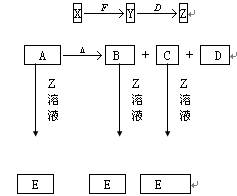
 知甲、乙、丙、X是4种中学化学中常见的物质,其转化关系符合下图。则甲和X(要求甲和X能互换)不可能是( )
知甲、乙、丙、X是4种中学化学中常见的物质,其转化关系符合下图。则甲和X(要求甲和X能互换)不可能是( ) 