题目内容
【题目】用NA表示阿伏伽德罗常数,下列说法中正确的是
A. 已知可将 0.1 mol NaCl 全部溶于乙醇中制成胶体,其中含有的胶体粒子数目为 0.1 NA
B. 标况下,0.5 mol CCl4的体积约为11.2 L
C. 常温常压下,14 g氮气中含有7NA个电子
D. 含NA个Na+的 Na2O溶解于1L水中,Na+的物质的量浓度为1molL-1
【答案】C
【解析】A、胶体是粒子的集合体,已知可将 0.1 mol NaCl 全部溶于乙醇中制成胶体,其中含有的胶体粒子数目小于 0.1 NA,选项A错误;B、标况下,气体摩尔体积为22.4L/mol,但CCl4为液态,无法用Vm=22.4L/mol计算,选项B错误;C、C. 常温常压下,14 g氮气中含有![]() ×2×NAmol-1=7NA个电子,选项C正确;C、含NA个Na+的 Na2O溶解于1L水中得到的溶液不为1L,无法计算Na+的物质的量浓度,选项D错误。答案选C。
×2×NAmol-1=7NA个电子,选项C正确;C、含NA个Na+的 Na2O溶解于1L水中得到的溶液不为1L,无法计算Na+的物质的量浓度,选项D错误。答案选C。

【题目】下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
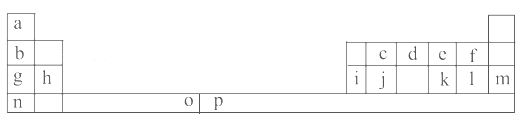
试回答下列问题:
(1)元素p为26号元素,请写出其原子的三价阳离子的电子排布式:______________。
(2)e与a反应的产物的分子中中心原子的杂化形式为__________,该分子是__________(填“极性”或“非极性”)分子。
(3)请写出f的氢化物在水中所存在氢键的表达式:(任写两种即可)_________________________。
(4)o、p两元素的部分电离能数据列于下表:
元素 | o | p | |
电离能 /kJ·mol-1 | I1 | 717 | 759 |
I2 | 1 509 | 1 561 | |
I3 | 3 248 | 2 957 | |
比较两元素的I2、I3可知,气态o2+再失去一个电子比气态p2+再失去一个电子难。对此,你的解释是___________________________________;
(5)i单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。
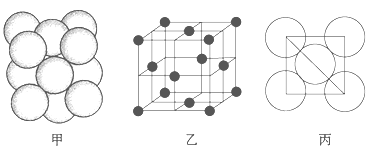
请问晶胞中i原子的配位数为________,一个晶胞中i原子的数目为________。