题目内容
在Na2S溶液中存在的下列关系不正确的是( )
A.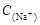 =2[ =2[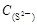 + +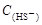 + +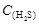 ] ] |
B.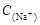 + +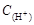 = =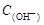 + +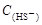 + +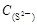 |
C.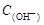 = =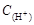 + +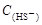 +2 +2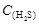 |
D.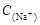 > >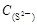 > >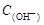 > >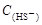 |
B
A符合物料守恒,正确。C符合质子守恒,正确。硫化钠水解显碱性,D正确。B不符合电荷守恒定律,是错误的,应该是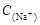 +
+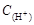 =
=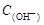 +
+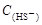 +2
+2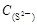 ,答案选B。
,答案选B。
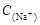 +
+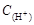 =
=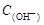 +
+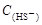 +2
+2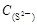 ,答案选B。
,答案选B。
练习册系列答案
相关题目
题目内容
A.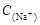 =2[ =2[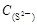 + +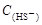 + +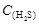 ] ] |
B.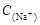 + +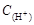 = =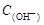 + +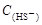 + +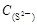 |
C.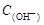 = =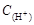 + +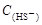 +2 +2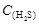 |
D.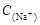 > >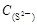 > >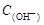 > >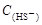 |
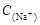 +
+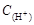 =
=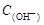 +
+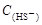 +2
+2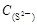 ,答案选B。
,答案选B。