题目内容
【题目】某小组探究用4HCl+O2![]() 2H2O+2Cl2的方法制取Cl2并验证其性质,设计实验如图所示(夹持装置略去)。请回答下列问题:
2H2O+2Cl2的方法制取Cl2并验证其性质,设计实验如图所示(夹持装置略去)。请回答下列问题:

(1)对装置B进行气密性检查的方法是____________。
(2)装置E中盛放无水CuSO4的仪器名称为_____;此装置的现象及作用是_______。
(3)设计实验检测上述方法得到的Cl2中是否含有HCl:__________。
(4)该小组用制得的Cl2和如图所给装置(不能重复使用)依次验证干燥纯净的Cl2无漂白性、湿润的Cl2有漂白性、Cl的非金属性强于S。按气流从左到右的方向,装置依次连接的合理顺序为F、___________、J。
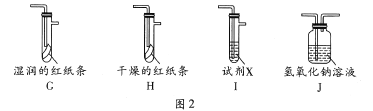
(5)若I中的试剂X为Na2S溶液,写出反应的离子方程式:________。”
(6)吸收尾气使用的是200mL 1.0 mol·L-1氢氧化钠溶液,配制此溶液需要的玻璃仪器有胶头滴管、玻璃棒、_______、________等。
【答案】 把导管伸入水中,给烧瓶微热,在导管口有气泡产生,冷却后在导管中形成一段水柱 干燥管 无水CuSO4变蓝说明装置D中有水生成,从而证明有Cl2生成 将生成的气体通入足量CCl4中后,再通入AgNO3溶液,若无白色沉淀生成,则气体中不含HCl;若有白色沉淀生成,则气体中含有HCl H、G、I Cl2+S2-=2Cl-+S↓ 250mL容量瓶 烧杯
【解析】试题分析:(1)把导管伸入水中,给烧瓶微热,在导管口有气泡产生,冷却后在导管中形成一段水柱说明气密性良好。
(2)根据图示回答装置E中盛放无水CuSO4的仪器名称;CuSO4遇水变蓝色。
(3)氯气、氯化氢与硝酸银溶液反应都能生成氯化银沉淀,检测得到的Cl2中是否含有HCl需先除去氯气;
(4)干燥的氯气通入干燥的红纸条验证干燥纯净的Cl2无漂白性、氯气通入湿润的红纸条证明湿润的Cl2有漂白性、氯气与硫化钠溶液反应生成硫沉淀可证明Cl的非金属性强于S,氯气有毒,最后用氢氧化钠进行尾气处理。
(5)氯气与硫化钠溶液反应生成硫沉淀和氯化钠。
(6)根据配制一定物质的量浓度的溶液分析需要的玻璃仪器。
解析:(1)把B中导管伸入水中,给烧瓶微热,在导管口有气泡产生,冷却后在导管中形成一段水柱说明B装置气密性良好。
(2)装置E中盛放无水CuSO4的仪器名称是干燥管;CuSO4遇水变蓝色,无水CuSO4变蓝说明装置D中有水生成,从而证明有Cl2生成。
(3)检测Cl2中是否含有HCl的方法是将生成的气体通入足量CCl4中后,再通入AgNO3溶液,若无白色沉淀生成,则气体中不含HCl;若有白色沉淀生成,则气体中含有HCl;
(4)干燥的氯气通入干燥的红纸条验证干燥纯净的Cl2无漂白性、氯气通入湿润的红纸条证明湿润的Cl2有漂白性、氯气与硫化钠溶液反应生成硫沉淀可证明Cl的非金属性强于S,氯气有毒,最后用氢氧化钠进行尾气处理,从左到右的方向,装置依次连接的合理顺序为F、H、G、I 、J。
(5)氯气与硫化钠溶液反应生成硫沉淀和氯化钠,反应离子方程式为Cl2+S2-=2Cl-+S↓。
(6)配制一定物质的量浓度的溶液,需要用烧杯溶解固体,用250mL容量瓶定容。

 阅读快车系列答案
阅读快车系列答案【题目】回答下列问题:
(1)某二元酸(分子式用H2B表示)在水中的电离方程式是:H2B===H++HB-;HB-![]() H++B2-。在0.1 mol/L的Na2B溶液中,下列粒子浓度关系式正确的是________。
H++B2-。在0.1 mol/L的Na2B溶液中,下列粒子浓度关系式正确的是________。
A.c(B2-)+c(HB-)=0.1 mol/L
B.c(B2-)+c(HB-)+c(H2B)=![]() c(Na+)
c(Na+)
C.c(OH-)=c(H+)+c(HB-)
D.c(Na+)+c(OH-)=c(H+)+c(HB-)
(2)下表为几种酸的电离平衡常数
CH3COOH | H2CO3 | H2S |
1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=9.1×10-8 K2=1.1×10-12 |
则pH相同的CH3COONa、Na2CO3、NaHS溶液物质的量浓度由大到小的顺序为________________,少量CO2与NaHS反应的离子方程式为______________。