题目内容
【题目】氯化亚铜(CuCl)常用作有机合成工业中的催化剂,在空气中迅速被氧化成绿色;见光则分解,变成褐色。下图是工业上用制作印刷电路的废液(含Fe3+、Cu2+、Fe2+、Cl-)生产CuCl的流程:
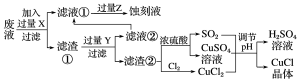
根据以上信息回答下列问题:
(1)写出生产过程中X___________,Y___________。
(2)写出产生CuCl的化学方程式:______________________。
(3)在CuCl的生成过程中理论上不需要补充SO2气体,结合化学方程式和必要的文字说明理由:________。
(4)在CuCl的生成过程中除环境问题、安全问题外,你认为还应该注意的关键问题是______________。
(5)实验探究pH对CuCl产率的影响如下表所示:
pH | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
CuCl产率 | 70 | 90 | 82 | 78 | 75 | 72 | 70 |
析出CuCl晶体最佳pH为___________,当pH较大时CuCl产率变低的原因是________________。
(6)氯化亚铜的定量分析:
①称取样品0.25 g和10 mL过量的FeCl3溶液于250 mL锥形瓶中,充分溶解。
②用0.10 mol·L-1硫酸铈[Ce(SO4)2]标准溶液滴定。已知:CuCl + FeCl3 === CuCl2 + FeCl2 、Fe2+ + Ce4+ === Fe3++ Ce3+。三次平行实验结果如下(平行实验结果相差不能超过1%):
平行实验次数 | 1 | 2 | 3 |
0.25 g样品消耗硫酸铈标准溶液的体积(mL) | 24.35 | 24.05 | 23.95 |
则样品中CuCl的纯度为___________(结果保留三位有效数字)。
【答案】(1)Fe 稀盐酸 (2)CuCl2+CuSO4+SO2+2H2O=2CuCl↓+2H2SO4
(3)反应Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O中生成的CuSO4和 SO2为1∶1,所以理论上不需要补充SO2气体 (4)生产中应防止CuCl的氧化和见光分解
CuSO4+SO2↑+2H2O中生成的CuSO4和 SO2为1∶1,所以理论上不需要补充SO2气体 (4)生产中应防止CuCl的氧化和见光分解
(5)2 pH较大时,Cu2+水解程度增大,反应生成的CuCl减少
(6)0.955(或95.5%)
【解析】
试题分析:(1)废液中含有Fe3+、Cu2+,应加入Fe除去,过量的Fe用稀盐酸除去,所以试剂X、Y分别是Fe、稀盐酸。
(2)由流程图可知,CuCl晶体的制备过程中,反应物为SO2、CuSO4、CuCl2,生成物为H2SO4、CuCl,由化合价升降守恒及原子守恒,可得反应方程式为CuCl2+CuSO4+SO2+2H2O=2CuCl↓+2H2SO4。
(3)由反应方程式Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O可知,Cu与浓硫酸反应的过程中有SO2生成,且生成的CuSO4和 SO2为1∶1,生产CuCl的过程中消耗CuSO4和SO2也为1∶1,所以理论上不需要补充SO2气体。
CuSO4+SO2↑+2H2O可知,Cu与浓硫酸反应的过程中有SO2生成,且生成的CuSO4和 SO2为1∶1,生产CuCl的过程中消耗CuSO4和SO2也为1∶1,所以理论上不需要补充SO2气体。
(4)因CuCl在空气中迅速被氧化成绿色且见光分解,变成褐色,故生产中应注意防止CuCl的氧化和见光分解。
(5)由表中数据可知,pH=2时,CuCl产率最高;pH较大时,Cu2+水解程度增大,导致反应生成的CuCl减少。
(6)滴定0.25 g样品消耗硫酸铈标准溶液的平均体积是24 mL,所以CuCl的纯度为![]() 。
。