题目内容
【题目】(Ⅰ)下列叙述正确的有_______________
A.第四周期元素中,锰原子价电子层中未成对电子数最多
B.第二周期主族元素的原子半径随核电荷数增大依次减小
C.卤素氢化物中,HCl的沸点最低的原因是其分子间的范德华力最小
(Ⅱ)M是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子。元素Y的负一价离子的最外层电子数与次外层的相同。回答下列问题:
(1)单质M的晶体类型为______,晶体中原子间通过_____作用形成面心立方密堆积,其中M原子的配位数为______。
(2)元素Y基态原子的核外电子排布式为________,其同周期元素中,第一电离能最大的是______(写元素符号)。元素Y的含氧酸中,酸性最强的是________(写化学式),该酸根离子的立体构型为________。
(3)M与Y形成的一种化合物的立方晶胞如图所示。
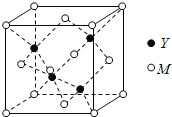
①该化合物的化学式为_______,已知晶胞参数a=0.542 nm,此晶体的密度为_______g·cm–3。(写出计算式,不要求计算结果。阿伏加德罗常数为NA)
②该化合物难溶于水但易溶于氨水,其原因是________。此化合物的氨水溶液遇到空气则被氧化为深蓝色,深蓝色溶液中阳离子的化学式为_______。
【答案】B 金属晶体 金属阳离子与自由电子之间的静电作用 12 1s22s22p63s23p5 Ar HClO4 正四面体 CuCl (64+35.5)×4/(a3×10-21×NA)g/cm3 Cu+可与氨形成易溶于水的配位化合物 [Cu(NH3)4]2+
【解析】
(Ⅰ)A.第四周期元素中,能级处于半满稳定状态时,含有的未成对电子数最多;
B.同周期元素,核电荷数越多半径越小;
C.HF分子间存在氢键,HCl分子间没有氢键,熔沸点低于HF;
(Ⅱ)M是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子,则M为Cu;元素Y的负一价离子的最外层电子数与次外层的相同,则Y为Cl;
(Ⅰ)A.第四周期元素中,外围电子排布为3dx3sy,且能级处于半满稳定状态时,含有的未成对电子数最多,则外围电子排布为3d54s1,此元素为铬,A错误;
B.同周期元素,核电荷数越多半径越小,则第二周期主族元素的原子半径随核电荷数增大依次减小,B正确;
C.HF分子间存在氢键,HCl分子间没有氢键,但HCl分子间的范德华力大于HF分子间的,C不正确;
答案为B;
(Ⅱ)M是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子,则M为Cu;元素Y的负一价离子的最外层电子数与次外层的相同,则Y为Cl;
(1)单质M为Cu,其晶体类型为为金属晶体;通过金属阳离子与自由电子之间的静电作用结合在一起,晶体为面心立方密堆积,Cu原子的配位数为12;
(2)元素Y为Cl,基态原子的核外电子排布式为1s22s22p63s23p5;同周期元素中,第一电离能最大的是Ar;元素Cl的含氧酸中,酸性最强的是HClO4;高氯酸酸根离子中氯原子没有孤对电子,为sp3杂化,立体构型为正四面体;
(3)①根据晶胞的图像,Cu原子在顶点和面心,按分摊法,Cu原子数目=8×1/8+6×1/2=4,Cl原子在体内,数目为4,两种原子的个数比为1:1,则其化学式为CuCl;ρ=m/V=(64+35.5)×4g/(a3nm×NA)=(64+35.5)×4/(a3×10-21×NA)g/cm3;
②Cu+可与氨形成易溶于水的配位化合物,所以CuCl难溶于水但易溶于氨水;该化合物中Cu+被空气中的氧气氧化为Cu2+,与氨水中的氨分子生成配离子,则深蓝色溶液中阳离子为:[Cu(NH3)4]2+。

【题目】现有部分元素的性质与原子(或分子)结构如下表:
元素编号 | 元素性质与原子(或分子)结构 |
T | 最外层电子数是次外层电子数的3倍 |
X | 常温下单质为双原子分子,分子中含有3对共用电子对 |
Y | M层比K层少1个电子 |
Z | 第3周期元素的简单离子中半径最小 |
(1)写出元素T的原子结构示意图____________________________
(2)元素Y与元素Z相比,金属性较强的是________(用元素符号表示)。
(3)X元素的气态氢化物溶于水后与其最高价氧化物对应水化物反应的离子方程式为__________。
(4)元素Y和硫元素可形成化合物Y2S,请用电子式表示该化合物的形成过程________