题目内容
11.有关难溶电解质沉淀溶解平衡的说法错误的是( )| A. | 难溶电解质沉淀的速率和溶解的速率相等 | |
| B. | 溶液中各离子的浓度不再改变 | |
| C. | 难溶电解质在水中形成饱和溶液 | |
| D. | 加水可使难溶电解质的KSP增大 |
分析 A、沉淀的速率和溶解的速率相等,沉淀溶解达到平衡;
B、达到平衡,溶液中各离子的浓度不再改变;
C、沉淀溶解达到平衡时,形成饱和溶液;
D、KSP只与温度有关.
解答 解:A、沉淀的速率和溶解的速率相等,沉淀溶解达到平衡,故A正确;
B、达到平衡,溶液中各离子的浓度不再改变,故B正确;
C、沉淀溶解达到平衡时,形成饱和溶液,故C正确;
D、KSP只与温度有关,加水可使难溶电解质的KSP不变,故D错误;
故选D.
点评 本题考查难溶物质的溶解平衡,难度不大,注意利用平衡移动原理、溶度积常数理解.

练习册系列答案
相关题目
6.已知常温下Cu(OH)2的溶度积为2.2×10-22,常温下,在0.20mol/LCuSO4溶液中加入NaOH溶液,充分搅拌,有浅蓝色沉淀Cu(OH)2生成,当溶液的pH=10时,溶液中的Cu2+的物质的量浓度为( )
| A. | 2.2×10-10 mol/L | B. | 2.2×10-12 mol/L | C. | 2.2×10-14 mol/L | D. | 1.1×10-21 mol/L |
16.下列说法中正确的是( )
| A. | 饱和石灰水中加入一定量生石灰,温度明显升高,所得溶液的pH增大 | |
| B. | AgCl悬浊液中存在平衡:AgCl(s)?Ag+(aq)+Cl-(aq),往其中加入少量NaCl粉末,平衡向左移动,溶液中离子的总浓度会减小 | |
| C. | 为减小洗涤过程中固体的损失,最好选用稀H2SO4代替H2O来洗涤BaSO4沉淀 | |
| D. | 硬水中含有较多的Ca2+、Mg2+、HCO3-、SO42-,加热煮沸可以完全除去其中的 Ca2+、Mg2+ |
3.某无色透明的强碱性的溶液中都能大量共存的离子组是( )
| A. | Fe2+ K+ S${O}_{4}^{2-}$ N${O}_{3}^{-}$ | B. | Mg2+ N${H}_{4}^{+}$ S${O}_{4}^{2-}$ Cl- | ||
| C. | Na+ K+ S${O}_{4}^{2-}$ N${O}_{3}^{-}$ | D. | Ba2+ Na+ Mn${O}_{4}^{-}$ S${O}_{4}^{2-}$ |
1.下列有关石油的炼制和煤的综合利用的说法正确的是( )
| A. | 石油的催化裂化是为了提高汽油等轻质油的产量和质量 | |
| B. | 石油裂解可得到汽油 | |
| C. | 煤的气化和液化均为物理变化 | |
| D. | 石油在分馏过程中最先得到的馏分是柴油 |

 ;其水溶液长期在空气中放置容易变浑浊,该变化体现出:S非金属性比O弱O(填“强”或“弱”).用原子结构解释原因:同主族元素最外层电子数相同,从上到下,电子层数增多,原子半径增大,得电子能力逐渐减弱.
;其水溶液长期在空气中放置容易变浑浊,该变化体现出:S非金属性比O弱O(填“强”或“弱”).用原子结构解释原因:同主族元素最外层电子数相同,从上到下,电子层数增多,原子半径增大,得电子能力逐渐减弱.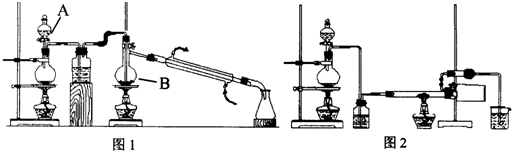
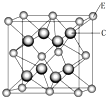 A、B、C、D、E、X六种元素的原子序数依次递增,A、B、C的基态原子中L层未成对电子数分别为3、2、1,D是短周期中原子半径最大的主族元素,E是主族元素且与X同周期,E与C可形成离子化合物,其晶胞结构如图所示.X位于元素周期表中第四周期ⅠB族.
A、B、C、D、E、X六种元素的原子序数依次递增,A、B、C的基态原子中L层未成对电子数分别为3、2、1,D是短周期中原子半径最大的主族元素,E是主族元素且与X同周期,E与C可形成离子化合物,其晶胞结构如图所示.X位于元素周期表中第四周期ⅠB族.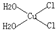 .
.