题目内容
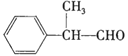
【题目】化合物![]() 与
与![]() 可以通过配位键形成
可以通过配位键形成![]() 。
。
(1)在![]() 中,___________________原子提供孤电子对,___________________原子接受孤电子对。
中,___________________原子提供孤电子对,___________________原子接受孤电子对。
(2)写出![]() 的结构式,并用“→”标出配位键:____________________。
的结构式,并用“→”标出配位键:____________________。
【答案】氮 硼 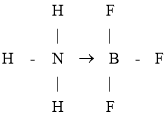
【解析】
(1)B原子含有3个σ 键、一个配位键,B原子提供空轨道的原子、N原子提供孤电子对;
(2)配位键有提供孤电子对的原子指向提供空轨道的离子。
(1)![]() 中B原子其价层电子数是4,采取sp3杂化,B原子含有3个σ键、一个配位键,该化合物中,B原子提供空轨道的原子、N原子提供孤电子对,B、N原子之间形成配位键,故答案为:氮;硼;
中B原子其价层电子数是4,采取sp3杂化,B原子含有3个σ键、一个配位键,该化合物中,B原子提供空轨道的原子、N原子提供孤电子对,B、N原子之间形成配位键,故答案为:氮;硼;
(2)![]() 中B原子提供空轨道的原子、N原子提供孤电子对,N→B,故结构式为:
中B原子提供空轨道的原子、N原子提供孤电子对,N→B,故结构式为: ,故答案为:
,故答案为: 。
。

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
【题目】按要求回答下列问题。
(1)下列基态原子或离子的电子排布式或轨道表示式正确的是_______(填序号,下同),违反能量最低原理的是_____,违反泡利不相容原理的是_____,违反洪特规则的是_______。
①Si:![]()
②Al:![]()
③Co3+最外层:![]()
④Mg2+:1s22s22p6
⑤Sc:1s22s22p63s23p63d3
⑥Cr:1s22s22p63s23p63d54s1
(2)物质:①甲烷 ②硫化氢 ③氢氧化镁 ④氨气 ⑤乙烯
条件 | 符合条件物质的序号 |
既含极性键又含非极性键 | ______ |
含有极性键的极性分子 | ______ |
上述分子中键角由大到小的顺序 | ______ |
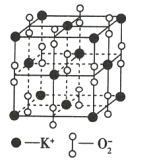
(3)甲图FeO晶胞中与Fe2+最近的Fe2+的个数为__________;乙图晶胞中A、B两种微粒个数比为______;丙图晶胞中A、B两种微粒个数比为_________。
甲. 乙.
乙.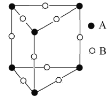 丙.
丙.