题目内容
国际能源网报道:金属燃料可能成为新能源,可能带来结束化石能源时代的希望,是一种理想的储能方式。下列说法不正确的是( )
| A.钠米金属燃料,更易点燃 |
| B.铁作燃料时,可用磁性材料吸引生成物,便于产物分离 |
| C.镁可以通过2Mg+CO2=2MgO+C,达到既节能减碳又释放能量的效果 |
| D.可从海水中提取氯化镁,并使氯化镁分解获得镁并释放出能量 |
D
解析

已知下列热化学方程式:Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g);△H="-24.8" kJ/mol
2Fe(s)+3CO2(g);△H="-24.8" kJ/mol
Fe2O3(s)+ 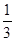 CO(g)
CO(g)
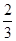 Fe3O4(s)+
Fe3O4(s)+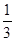 CO2(g);△H="-15.73" kJ/mol
CO2(g);△H="-15.73" kJ/mol
Fe3O4(s)+ CO(g) 3FeO(s)+CO2(g);△H="+640.4" kJ/mol
3FeO(s)+CO2(g);△H="+640.4" kJ/mol
则14 g CO气体还原足量FeO固体得到Fe固体和CO2气体时对应的ΔH约为 ( )
| A.-218 kJ/mol | B.-109 kJ/mol | C.+218 kJ/mol | D.+109 kJ/mol |
石墨和金刚石都是碳的单质,石墨在一定条件下可转化为金刚石。已知12 g石墨完全转化成金刚石时,要吸收1.9 kJ的能量。下列说法正确的是( )
| A.石墨不如金刚石稳定 |
| B.由金刚石制备石墨是吸热反应 |
| C.等质量的石墨与金刚石完全燃烧,金刚石放出的能量更多 |
| D.等质量的石墨与金刚石完全燃烧,石墨放出的能量更多 |
下列反应过程中的能量变化与下图一致的是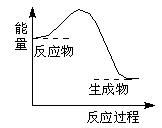
A.2Al+Fe2O3 2Fe+Al2O3 2Fe+Al2O3 |
B.C+CO2 2CO 2CO |
C.CaCO3 CaO+CO2↑ CaO+CO2↑ |
D.C+H2O CO+H2 CO+H2 |
已知断开1 mol H2中的化学键需要吸收436kJ的能量,断开1 mol Cl2中的化学键需要吸收243kJ的能量,而形成1mol HCl分子中的化学要释放431kJ的能量,则1mol氢气与1mol氯气反应时能量变化为
| A.吸收183kJ | B.吸收366kJ | C.放出183kJ | D.放出366kJ |
某学生实验小组用50 mL 0.50 mol·L-1的盐酸与50 mL 0.50 mol·L-1的NaOH溶液在右图所示的装置中进行中和反应反应热的测定。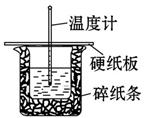
(1)图中装置缺少一种仪器,该仪器名称为______。
(2)下列说法正确的是______。
| A.小烧杯内残留有水,会使测得的反应热数值偏小 |
| B.酸、碱混合时,应把量筒中的溶液缓缓倒入烧杯的溶液中,以防液体外溅 |
| C.烧杯间填满碎纸条的作用是固定小烧杯 |
| D.可用相同浓度和体积的硝酸代替稀盐酸溶液进行实验 |
下列不属于生物质能的利用的是
| A.燃烧树枝取热 | B.将植物秸杆制沼气 |
| C.用淀粉制乙醇 | D.用太阳能发电 |
已知热化学方程式:SO2(g)+ 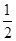 O2(g)
O2(g) 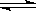 SO3(g) △H = ―98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为( )
SO3(g) △H = ―98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为( )
| A.196.64kJ | B.196.64kJ/mol | C.<196.64kJ | D.>196.64kJ |
下列与化学反应能量变化相关的叙述正确的是( )
| A.生成物总能量一定低于反应物总能量 |
| B.等量H2在O2中完全燃烧生成H2O(g)与生成H2O(l),放出的能量相同 |
| C.应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| D.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH不同 |