题目内容
【题目】某课外活动小组的同学在学习了电化学相关知识后,用如图装置进行实验,请回答下列问题:
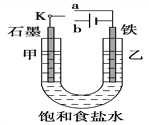
(1)实验一:将开关K与a连接,则乙的电极反应式为___。
(2)实验二:开关K与b连接,则总反应的离子方程式为_______。
(3)对于实验二,下列说法正确的是___(填字母)。
A.溶液中Na+向甲极移动
B.从甲极处逸出的气体能使湿润的KI淀粉试纸变蓝
C.反应一段时间后加适量HCl可恢复到电解前电解质的浓度
D.反应在结束后,甲电极和乙电极上收集到的气体体积一定相等
【答案】 Fe-2e-=Fe2+ 2Cl-+2H2O=2OH-+H2↑+Cl2↑ B
【解析】(1)开始时开关K与a连接,是原电池,铁为负极,发生氧化反应,失去电子生成亚铁离子,电极方程式为Fe-2e-=Fe2+,甲电极上氧气得电子被还原,电极方程式为O2+2H2O+4e-=4OH-,故答案为:Fe-2e-=Fe2+;
(2)开关K与b连接,装置为电解池,铁为阴极,发生还原反应,氢离子得到电子生成氢气,总反应为电解饱和食盐水生成氢氧化钠、氢气和氯气,总反应式为2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑,离子方程式为2Cl-+2H2O=2OH-+H2↑+Cl2↑,故答案为:2Cl-+2H2O=2OH-+H2↑+Cl2↑;
2NaOH+H2↑+Cl2↑,离子方程式为2Cl-+2H2O=2OH-+H2↑+Cl2↑,故答案为:2Cl-+2H2O=2OH-+H2↑+Cl2↑;
(3)A.溶液中Na+向阴极乙极移动,故错误;B.从甲极处逸出的气体为氯气,能使湿润KI淀粉试纸变蓝,故正确;C.电解饱和食盐水实质为电解氯化氢,因为盐酸为氯化氢的水溶液,所以反应一段时间后加适量盐酸不可恢复到电解前电解质的浓度,故错误;D. 反应在结束后,甲电极收集到的气体为氯气,乙电极收集到的气体为氢气,由于氯气能够与生成的氢氧化钠反应,导致生成的氯气和氢气的体积不相等,故错误;故选B。

【题目】四个电解装置都以Pt作电极,它们分别装着如下电解质溶液进行电解,电解一段时间后,测定其pH变化,所记录的结果正确的是
选项 | A | B | C | D |
电解质溶液pH 变化 | HCl | AgNO3 | KOH | BaCl2 |
pH变化 | 减小 | 增大 | 增大 | 不变 |
A. A B. B C. C D. D