题目内容
下列有关反应限度的叙述正确的是
| A.大多数化学反应在一定条件下都有一定的限度 |
| B.依据焓判据:NH4HCO3受热分解可自发进行 |
| C.使用催化剂,既能加快反应速率,又能改变反应限度 |
| D.平衡常数K的大小能说明反应的限度,因此当平衡右移时,K值必定增大 |
A
反应自发进行的判据是:△H-T△S<0,故B错误;
使用催化剂,只能加快反应速率,不能改变反应限度,故C错误;
K值增大还是减小,与反应的热效应有关,故D错误
使用催化剂,只能加快反应速率,不能改变反应限度,故C错误;
K值增大还是减小,与反应的热效应有关,故D错误

练习册系列答案
相关题目
 的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
的混合溶液可溶出印刷电路板金属粉末中的铜。已知: ====
==== △H=+64kJ/mol
△H=+64kJ/mol ====
==== △H= -196kJ/mol
△H= -196kJ/mol ="==="
="==="  △H= -286kJ/mol
△H= -286kJ/mol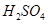 溶液中
溶液中 与
与 反应生成
反应生成 和
和 的热化学方程式为 。
的热化学方程式为 。 和3.0 mol/L的
和3.0 mol/L的 )
) 溶液中加入一定量的
溶液中加入一定量的 和
和 溶液,加热,生成
溶液,加热,生成 沉淀。制备
沉淀。制备 键分别需要的能是436kJ、39lkJ、946kJ,则N2与H2反应生成NH3的热化学方程式为________________________________。
键分别需要的能是436kJ、39lkJ、946kJ,则N2与H2反应生成NH3的热化学方程式为________________________________。
