题目内容
1.下列现象或事实可以用同一原理解释的是( )| A. | 浓硫酸和浓盐酸长期露置在空气中浓度均降低 | |
| B. | 氯化铵和碘都可以用加热的方法进行提纯 | |
| C. | 氯水、SO2均能使品红溶液褪色 | |
| D. | 溴蒸汽和NO2气体都能使湿润的淀粉碘化钾试纸变蓝 |
分析 A.浓硫酸具有吸水性、浓盐酸具有挥发性;
B.氯化铵加热分解、碘加热升华;
C.氯水有强氧化性,二氧化硫能与品红结合生成无色物质;
D.溴、二氧化氮都具有强的氧化性,能够氧化碘离子生成单质碘.
解答 解:A.浓硫酸露置空气中吸收空气中的水,溶液浓度降低,盐酸易挥发导致浓度均降低,但原理不同,故A错误;
B.氯化铵加热分解、碘加热升华,所以不能用加热法进行提纯,故B错误;
C.氯水有强氧化性,能将品红氧化成无色物质,二氧化硫能与品红结合生成无色物质,故C错误;
D.溴、二氧化氮都具有强的氧化性,能够氧化碘离子生成单质碘,碘遇到淀粉变蓝,故D正确;
故选:D.
点评 本题考查物质的性质,题目难度不大,注意氯水有强氧化性,能将品红氧化成无色物质,二氧化硫能与品红结合生成无色物质,注意溴、二氧化氮的强的氧化性,题目难度不大.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
11.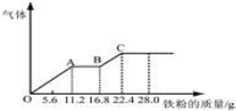 某稀硫酸和稀硝酸的混合溶液 200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解 19.2g(已知硝酸只被还原为 NO 气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示. 下列分析或结果正确的是( )
某稀硫酸和稀硝酸的混合溶液 200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解 19.2g(已知硝酸只被还原为 NO 气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示. 下列分析或结果正确的是( )
 某稀硫酸和稀硝酸的混合溶液 200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解 19.2g(已知硝酸只被还原为 NO 气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示. 下列分析或结果正确的是( )
某稀硫酸和稀硝酸的混合溶液 200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解 19.2g(已知硝酸只被还原为 NO 气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示. 下列分析或结果正确的是( )| A. | 每份溶液中NO-3物质的量为 0.4mol | |
| B. | 原溶液中H2SO4浓度为2.5mol•L-1 | |
| C. | 第一份溶液中最终溶质为CuSO4和 Cu(NO3)2 | |
| D. | OA段产生的是NO,AB段的反应为Fe+2Fe3+═Fe2+,BC段产生氢气 |
12.下列说法正确的是( )
| A. | 所有自发进行的反应都是放热反应 | |
| B. | 同一物质固、液、气三种状态的熵值相同 | |
| C. | 恒温恒压下,△H<0且△S>0的反应一定可以自发进行 | |
| D. | 自发反应在任何条件下都能实现 |
16.下列与实验相关的叙述,正确的是( )
| A. | 浓硝酸存放在带橡胶塞的棕色玻璃瓶中 | |
| B. | 四氯化碳萃取溴水中的溴时,水从分液漏斗下口流出 | |
| C. | 向饱和的NaCl溶液中通入足量的NH3后,再通入CO2,有晶体析出 | |
| D. | 某溶液中滴加BaCl2溶液,产生不溶于稀硝酸的白色沉淀,该溶液中一定含有Ag+ |
13.晚自习的课间,同学们站在四楼上,可以看到市里的空中有移动的光柱,这就是气溶胶发生的丁达尔效应,下列说法不正确的是( )
| A. | 制备Fe(OH)3胶体的化学方程式是FeCl3+3H2O$\frac{\underline{\;煮沸\;}}{\;}$Fe(OH)3↓+3HCl | |
| B. | 胶体分散质粒子的直径介于1~100nm之间 | |
| C. | 利用丁达尔效应可鉴别胶体和溶液 | |
| D. | 胶体和溶液都是混合物,它们属于不同的分散系 |
10.1g N2含有x个N2,则阿伏加德罗常数为( )
| A. | $\frac{x}{28}$ | B. | 14x mol-1 | C. | 28x mol-1 | D. | 28x |
11.下列有关反应热的说法正确的是( )
| A. | 在化学反应过程中,吸热反应需不断从外界获得能量,放热反应不需从外界获得能量 | |
| B. | 由C(石墨,S)═C(金刚石,S)△H=+1.9kJ•mol-1,可知金刚石比石墨稳定 | |
| C. | 已知常温常压下:HCl(aq)+NaOH(aq)=NaCl(aq)+H2O(l)△H=-57.3 kJ•mol-1,则有:H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l)△H=-114.6 kJ•mol-1 | |
| D. | 已知:S(s)+O2(g)=SO2(g)△H1=-Q1 kJ•mol-1,S(g)+O2(g)=SO2(g)△H2=-Q2kJ•mol-1,则Q1<Q2 |
 .
.