题目内容
向反应体系中同时通入甲烷、氧气和水蒸气,发生的主要化学反应有:I.CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H1=-802.6kJ/mol
II.CH4(g)+O2(g)═CO2(g)+2H2(g)△H2=-322.0kJ/mol
III.CH4(g)+H2O(g)═CO(g)+3H2(g)△H3=+206.2kJ/mol
Ⅳ.CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H4=+165.0kJ/mol
请回答下列问题:
(1)CH4的燃烧热△H______△H1.(填“>”、“<”或“=”).
(2)在反应初始阶段,反应II的反应速率大于反应III的反应速率.比较反应II的活化能EII和反应III的活化能EIII的大小:EII______EIII(填“>”、“<”或“=”).
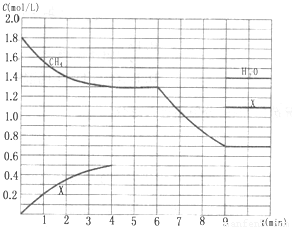
(3)在1L固定容积密闭容器中投入1.8mol CH4和3.6mol H2O(g),若只发生反应Ⅳ,测得CH4、H2O(g)及某一生成物的物质的量浓度(c)随反应时间(t)的变化如图所示[第9min前H2O(g)的物质的量浓度及第4min~9min之间X所代表生成物的物质的量浓度变化曲线未标出,条件有变化时只考虑改变一个条件).
①0~4min内,H2的平均反应速率υ(H2)=______mol?-1;
②反应在5min时的平衡常数K=______;
③第6min时改变的条件是______;判断理由是______;
④比较第5min时的平衡常数K5min与第10min时平衡常数K10min的大小:K5min______K10min (填“>”、“=”或“<”),原因是______.
【答案】分析:(1)反应生成液态水放出的热量更多;
(2)活化能越低,反应速率越快,初始阶段,反应II的反应速率大于反应III的反应速率;
(3)根据图象0-4min甲烷减少0.5mol/L,X增加0.5mol/L,则X为二氧化碳,4-6min为平衡状态,
CH4(g)+2H2O(g)═CO2(g)+4H2(g)
开始 1.8 3.6 0 0
转化 0.5 1 0.5 2
平衡 1.3 2.6 0.5 2
结合温度对反应速率的影响来解答.
解答:解:(1)反应生成液态水放出的热量更多,则CH4的燃烧热△H<△H1,故答案为:<;
(2)活化能越低,反应速率越快,初始阶段,反应II的反应速率大于反应III的反应速率,则反应II的活化能EII<反应III的活化能EIII,故答案为:<;
(3)根据图象0-4min甲烷减少0.5mol/L,X增加0.5mol/L,则X为二氧化碳,4-6min为平衡状态,
CH4(g)+2H2O(g)═CO2(g)+4H2(g)
开始 1.8 3.6 0 0
转化 0.5 1 0.5 2
平衡 1.3 2.6 0.5 2
①0~4min内,H2的平均反应速率υ(H2)=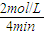 =0.5mol?L-1?min-1,故答案为:0.5;
=0.5mol?L-1?min-1,故答案为:0.5;
②反应在5min时的平衡常数K=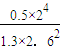 =0.91,故答案为:0.91;
=0.91,故答案为:0.91;
③根据图象第6 min~9 min时的反应速率比0~4 min时的大,且平衡向正反应方向移动,说明第6 min改变的条件为升高温度或增加水蒸气的量,再根据第9 min平衡时甲烷浓度为0.7 mol/L,水蒸气浓度为1.4 mol/L,说明甲烷消耗1.1 mol,水蒸气消耗2.2 mol,所以不可能为增加水蒸气的量,因此改变的条件只可能为升高温度,
故答案为:升高温度;第6 min~9 min时的反应速率比0~4 min时的大,且平衡向正反应方向移动,说明第6 min改变的条件为升高温度或增加水蒸气的量,再根据第9 min平衡时甲烷浓度为0.7 mol/L,水蒸气浓度为1.4 mol/L,说明甲烷消耗1.1 mol,水蒸气消耗2.2 mol,所以不可能为增加水蒸气的量,因此改变的条件只可能为升高温度;
④因正反应为吸热反应,升高温度平衡常数增大,则K5min<K10min,故答案为:<;正反应为吸热反应,升高温度平衡常数增大.
点评:本题考查热化学以及化学反应速率、化学平衡等,意在考查考生分析、处理数据和解答图象试题的能力,解答本题需利用盖斯定律,联系化学平衡、化学平衡常数以及平衡移动原理等,弄清图象的含义,题目难度较大.
(2)活化能越低,反应速率越快,初始阶段,反应II的反应速率大于反应III的反应速率;
(3)根据图象0-4min甲烷减少0.5mol/L,X增加0.5mol/L,则X为二氧化碳,4-6min为平衡状态,
CH4(g)+2H2O(g)═CO2(g)+4H2(g)
开始 1.8 3.6 0 0
转化 0.5 1 0.5 2
平衡 1.3 2.6 0.5 2
结合温度对反应速率的影响来解答.
解答:解:(1)反应生成液态水放出的热量更多,则CH4的燃烧热△H<△H1,故答案为:<;
(2)活化能越低,反应速率越快,初始阶段,反应II的反应速率大于反应III的反应速率,则反应II的活化能EII<反应III的活化能EIII,故答案为:<;
(3)根据图象0-4min甲烷减少0.5mol/L,X增加0.5mol/L,则X为二氧化碳,4-6min为平衡状态,
CH4(g)+2H2O(g)═CO2(g)+4H2(g)
开始 1.8 3.6 0 0
转化 0.5 1 0.5 2
平衡 1.3 2.6 0.5 2
①0~4min内,H2的平均反应速率υ(H2)=
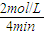 =0.5mol?L-1?min-1,故答案为:0.5;
=0.5mol?L-1?min-1,故答案为:0.5; ②反应在5min时的平衡常数K=
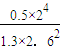 =0.91,故答案为:0.91;
=0.91,故答案为:0.91; ③根据图象第6 min~9 min时的反应速率比0~4 min时的大,且平衡向正反应方向移动,说明第6 min改变的条件为升高温度或增加水蒸气的量,再根据第9 min平衡时甲烷浓度为0.7 mol/L,水蒸气浓度为1.4 mol/L,说明甲烷消耗1.1 mol,水蒸气消耗2.2 mol,所以不可能为增加水蒸气的量,因此改变的条件只可能为升高温度,
故答案为:升高温度;第6 min~9 min时的反应速率比0~4 min时的大,且平衡向正反应方向移动,说明第6 min改变的条件为升高温度或增加水蒸气的量,再根据第9 min平衡时甲烷浓度为0.7 mol/L,水蒸气浓度为1.4 mol/L,说明甲烷消耗1.1 mol,水蒸气消耗2.2 mol,所以不可能为增加水蒸气的量,因此改变的条件只可能为升高温度;
④因正反应为吸热反应,升高温度平衡常数增大,则K5min<K10min,故答案为:<;正反应为吸热反应,升高温度平衡常数增大.
点评:本题考查热化学以及化学反应速率、化学平衡等,意在考查考生分析、处理数据和解答图象试题的能力,解答本题需利用盖斯定律,联系化学平衡、化学平衡常数以及平衡移动原理等,弄清图象的含义,题目难度较大.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
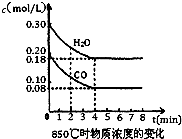 已知反应:CO(g)+H2O(g)?H2(g)+CO2(g)△H=-41.2kJ/mol,生成的CO2与H2以不同的体积比混合时在合适条件下的反应可制得CH4.
已知反应:CO(g)+H2O(g)?H2(g)+CO2(g)△H=-41.2kJ/mol,生成的CO2与H2以不同的体积比混合时在合适条件下的反应可制得CH4.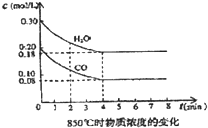 在一体积为10L的容器中,通入一定量的CO和H2O,在85℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H=-Q kJ/mol CO和H2O浓度变化如图,则
在一体积为10L的容器中,通入一定量的CO和H2O,在85℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H=-Q kJ/mol CO和H2O浓度变化如图,则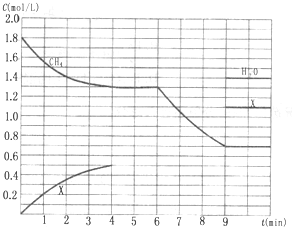 向反应体系中同时通入甲烷、氧气和水蒸气,发生的主要化学反应有:
向反应体系中同时通入甲烷、氧气和水蒸气,发生的主要化学反应有: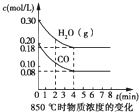 某研究小组利用反应CO(g)+H2O(g)?CO2(g)+2H2(g)△H=-41.2kJ/mol,制备CO2与H2的混合气体,并进一步研究CO2与H2以不同的体积之比混合时在合适条件下的反应情况.请回答下列问题:
某研究小组利用反应CO(g)+H2O(g)?CO2(g)+2H2(g)△H=-41.2kJ/mol,制备CO2与H2的混合气体,并进一步研究CO2与H2以不同的体积之比混合时在合适条件下的反应情况.请回答下列问题: