题目内容
下图中,A为气体非金属单质,N、P是金属单质;N可以在CO2中燃烧,P是日常生活中最常见的金属,D是空气中含量最多的气体;B、E、Z为无色氢化物。其中B、E为有刺激性气味的气体,Z为液体;C是由三种短周期非金属元素组成的离子化合物,F、I、L为白色沉淀,其中F不溶于稀硝酸;反应②在E的浓溶液中进行,反应⑦在E的稀溶液中进行,反应②、⑦均可用于实验室制取某种气体(图中部分反应物和生成物没有列出)。

请按要求回答:
(1)写出D的结构式____________,F的化学式____________;
(2)反应③的化学方程式为________________________;
(3)反应②的离子方程式为________________________;
(4)由J制取L时反应的环境要求是________________________。
(1)写出D的结构式____________,F的化学式____________;
(2)反应③的化学方程式为________________________;
(3)反应②的离子方程式为________________________;
(4)由J制取L时反应的环境要求是________________________。
(1)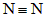 ;
;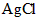
(2)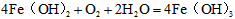
(3)
(4) 无氧
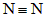 ;
;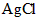
(2)
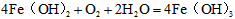
(3)

(4) 无氧

练习册系列答案
相关题目
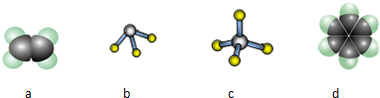
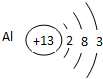
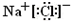


 元素原子的最外层电子数是其次外层电子数的=3/4倍;C与E同主族。
元素原子的最外层电子数是其次外层电子数的=3/4倍;C与E同主族。

 反应。
反应。