题目内容
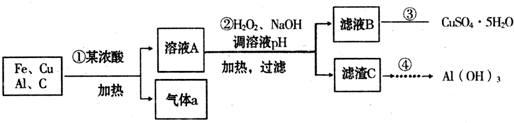
废弃物的综合利用既有利于节约资源,又有利于保护环境。实验室利用废旧黄铜(Cu、Zn合金,含少量杂质Fe)制备胆矾晶体(CuSO4·5H2O)及副产物ZnO。制备流程图如下:
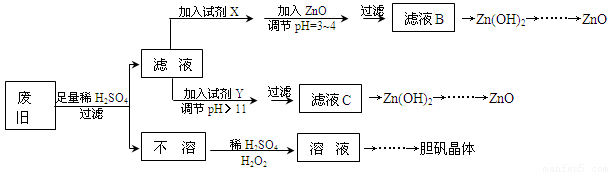
已知:Zn及化合物的性质与Al及化合物的性质相似,pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-。下表列出了几种离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol·L-1计算)。
| Fe3+ | Fe2+ | Zn2+ |
开始沉淀的pH | 1.1 | 5.8 | 5.9 |
沉淀完全的pH | 3.0 | 8.8 | 8.9 |
请回答下列问题:
(1)试剂X可能是__________,其作用是____________________。
(2)加入ZnO调节pH=3~4的目的是____________________。
(3)由不溶物生成溶液D的化学方程式为______________________________。
(4)由溶液D制胆矾晶体包含的主要操作步骤是______________________________。
(5)下列试剂可作为Y试剂的是______。
A.ZnOB.NaOHC.Na2CO3D.ZnSO4
若在滤液C中逐滴加入盐酸直到过量,则产生的现象是______________________________。
(6)测定胆矾晶体的纯度(不含能与I-发生反应的氧化性杂质):准确称取0.5000g胆矾晶体置于锥形瓶中,加适量水溶解,再加入过量KI,用0.1000mol·L-1Na2S2O3标准溶液滴定至终点,消耗Na2S2O3标准溶液19.40mL。已知:上述滴定过程中的离子方程式如下:
2Cu2++4I-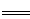 2CuI(白色)↓+I2,I2+2S2O32-
2CuI(白色)↓+I2,I2+2S2O32- 2I-+S4O62-
2I-+S4O62-
①胆矾晶体的纯度为_______________。
②在滴定过程中剧烈摇动(溶液不外溅)锥形瓶,则所测得的纯度将会__________(填“偏高”、“偏低”或“不变”)。
(1)H2O2 (新制氯水等氧化剂,其它合理答案也给分)(1分),将 Fe2+ 氧化为 Fe3+(2分)
(2)与H+ 反应,降低H+浓度,促使Fe3+彻底水解生成 Fe(OH)3沉淀而除去。(2分)
(3)Cu+H2O2+H2SO4 =CuSO4+2H2O(2分)
(4)蒸发浓缩、冷却结晶、抽滤(2分)
(5)B(1分),先产生白色沉淀后溶解(1分)(6)①97.00% (2分)②偏高(2分)
【解析】
试题分析:(1)废旧黄铜加足量稀硫酸,过滤,滤液中含有Fe2+、Fe3+、Zn2+,不溶物是铜。试剂X的作用是将Fe2+氧化成Fe3+,所以选择绿色氧化剂双氧水。
(2)加入ZnO调节pH=3~4的目的是与H+ 反应,降低H+浓度,促使Fe3+彻底水解生成 Fe(OH)3沉淀而除去;
(3)根据不溶物是铜,目的是制备胆矾,写出方程式Cu+H2O2+H2SO4 =CuSO4+2H2O;
(4)从溶液中分离出硫酸铜晶体应为蒸发浓缩、冷却结晶、抽滤;
(5)因为pH>11,Y试剂的目的是让Zn(OH)2全部生成[Zn(OH)4]2-,所以Y试剂选用NaOH,滤液C的主要成分是[Zn(OH)4]2-,逐滴加入盐酸直到过量,跟AlO2-溶液中逐滴加入盐酸直到过量进行类推,所以产生的现象是先产生白色沉淀后溶解;
(6)①2 CuSO4·5H2O?? ~????? 2Cu2+? ~??? I2???? ~???? 2S2O32-
???? 1.94×10-3mol????????????????????????????? 19.40mL×10-3×0.1000mol·L-1?????
胆矾晶体的质量 1.94×10-3mol ×250g·mol-1=0.485g
胆矾晶体的纯度为0.485g/0.5000g=97.00%
②因为滴定过程中剧烈摇晃锥形瓶会使一部分滴定液残留在玻璃壁上,导致滴定过程中消耗更多的滴定液,所以测得的纯度也会偏高。
考点:本题考查化学工业流程。

 阅读快车系列答案
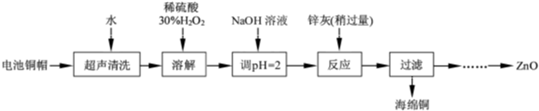
阅读快车系列答案[2012·江苏卷] (14分)废弃物的综合利用既有利于节约资源,又有利于保护环境。实验室利用废旧电池的铜帽(Cu、Zn总含量约为99%)回收 Cu并制备ZnO的部分实验过程如下: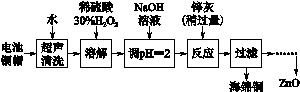
(2)①铜帽溶解时加入H2O2的目的是______ _____________________(用化学方程式表示)。
②铜帽溶解完全后,需将溶液中过量的H2O2除去。除去H2O2的简便方法____ ___。
(3)为确定加入锌灰(主要成分为Zn、ZnO,杂质为铁及其氧化物)的量,实验中需测定除去H2O2后溶液中Cu2+的含量。实验操作为:准确量取一定体积的含有Cu2+的溶液于带塞锥形瓶中,加适量水稀释,调节溶液pH=3~4,加入过量的KI,用Na2S2O3标准溶液滴定至终点。上述过程中反应的离子方程式如下:
2Cu2++4I-===2CuI(白色)↓+I2
2S2O32-+I2===2I-+S4O62-
①滴定选用的指示剂为________,滴定终点观察到的现象____________________。
②若滴定前溶液中的H2O2没有除尽,所测定的Cu2+含量将会________(填“偏高”、“偏低”或“ 不变”)。
已知pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-。下表列出了几种离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算)。
| | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Zn2+ | 5.9 | 8.9 |
由除去铜的滤液制备ZnO的实验步骤依次为:
①____________________________________________________________;
②__________________________________________________________________;
③过滤;
④___________________________________________________________________;
⑤过滤、洗涤、干燥;
⑥900 ℃煅烧。
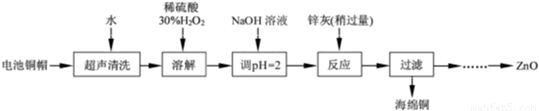
(1)①铜帽溶解时加入H2O2 的目的是 (用化学方程式表示).②铜帽溶解完全后,需将溶液中过量的H2O2 除去.除去H2O2 的简便方法是 .
(2)为确定加入锌灰(主要成分为Zn、ZnO,杂质为铁及其氧化物)的量,实验中需测定除去H2O2 后溶液中Cu2+的含量.实验操作为:准确量取一定体积的含有Cu2+的溶液于带塞锥形瓶中,加适量水稀释,调节溶液pH=3~4,加入过量的KI,用Na2S2O3标准溶液滴定至终点.上述过程中反应的离子方程式如下:摇摇2Cu2++4I-=2CuI(白色)↓+I2 2S2O32-+I2=2I-+S4O62-
①滴定选用的指示剂为 ,滴定终点观察到的现象为 .
②若滴定前溶液中的H2O2 没有除尽,所测定的Cu2+含量将会 (填“偏高”、“偏低”或“不变”).
(3)已知pH>11 时Zn(OH)2 能溶于NaOH溶液生成[Zn(OH)4]2-.下表列出了几种离子生成氢氧化物沉淀的pH.
| 开始沉淀的pH | 沉淀完全的pH | |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Zn2+ | 5.9 | 8.9 |
① ;② ;③过滤;④ ;⑤过滤、洗涤、干燥;⑥900℃煅烧.