题目内容
(9分)一定条件下,在一容积可变的密闭容器中,反应: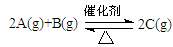 过程中的能量变化如图所示。反应过程中,A、B、C的物质的量(mol)的变化如下表:
过程中的能量变化如图所示。反应过程中,A、B、C的物质的量(mol)的变化如下表:
|
时间(min) |
0 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
n(A) |
2.00 |
1.90 |
1.82 |
1.76 |
1.64 |
1.54 |
1.50 |
1.50 |
1.50 |
|
n(B) |
1.00 |
0.95 |
0.91 |
0.88 |
0.82 |
0.77 |
0.75 |
0.75 |
0.75 |
|
n(C) |
0 |
0.10 |
0.18 |
0.24 |
0.36 |
0.46 |
0.50 |
0.50 |
0.50 |
回答下列问题:
(1)反应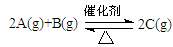 的正反应△H (填“大于”或“小于”)0。
的正反应△H (填“大于”或“小于”)0。
(2)该反应平衡时,下列说法不正确的是
(A)气体的密度不再改变 (B)A的物质的量浓度不变
(C)放出或吸收的热量不再变化 (D)v正(A)=v逆(A)=0
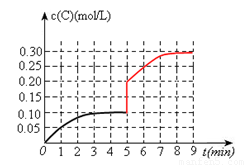
(3)toC时,在一容积为2L的恒容密闭容器内加入0.4molA和0.6molB,在一定条件下发生反应,反应中C的物质的量浓度变化情况如下图:
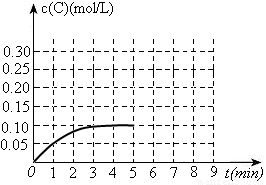
①该温度下,反应: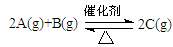 的平衡常数K=
。
的平衡常数K=
。
②反应进行到1分钟时B物质的量为 。
③在第5min时,将容器的体积缩小一半后,若在第8min达到新的平衡时A的总转化率为75%,请在上图中画出第5min到新平衡时C的物质的量浓度的变化曲线。
(共9分)
(1)< (2)D (3)① 4 ②0.55mol ③画图
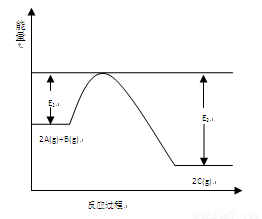
【解析】(1)产物总能量小于反应物总能量,故正反应是放热反应,△H<0
(2)化学平衡是一动态平衡,v正(A)=v逆(A)≠0
(3)①由图可知,平衡时c(C)=0.1mol/L,由方程式可求出c(A)、c(B)分别为0.1mol/L、0.25mol/L,进而可求出K=4
②由图可知,反应进行到1分钟时c(C)=0.05mol/L,即0.1mol,可求出B消耗了0.05mol;还剩余0.55mol
③在第5min时,将容器的体积缩小一半,c(C)瞬间增大一倍,即0.2mol/L;在第8min达到新的平衡时A的总转化率为75%,则可求出生成C为0.3mol,c(C)=0.3mol/L。

在一定条件下,在一容积可变的密闭容器中,将SO2和O2混合发生反应:
2SO2(g)+O2(g)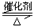 2SO3(g)
ΔH=-92.3KJ/mol,反应过程中,SO2、O2、SO3的物质的量(mol)的变化如下表(0~4min时,容器气体压强为0.1MPa):
2SO3(g)
ΔH=-92.3KJ/mol,反应过程中,SO2、O2、SO3的物质的量(mol)的变化如下表(0~4min时,容器气体压强为0.1MPa):
|
时间min |
0 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
|
n(SO2) |
2.00 |
1.92 |
1.84 |
1.76 |
1.76 |
1.64 |
1.52 |
1.40 |
1.40 |
1.40 |
|
n(O2) |
1.00 |
0.96 |
0.92 |
0.88 |
0.88 |
0.82 |
0.76 |
0.70 |
0.70 |
0.70 |
|
n(SO3) |
0 |
0.08 |
0.16 |
0.24 |
0.24 |
0.36 |
0.48 |
0.60 |
0.60 |
0.60 |
回答下列问题:
(1)___________________________时段,反应处于平衡状态。
(2)第5min时,从同时提高速率和转化率两个方面分析,改变的外界条件是_____________;平衡向____________方向移动。(填“正”、“逆”或“不”)
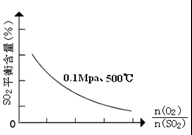
(3)其他条件相同、催化剂不同时,SO2的转化率随反应温度的变化如图a。,Fe2O3和NiO作催化剂均能使S02的转化率达到最高,不考虑价格因素,选择Fe2O3的 主要优点是_____________。
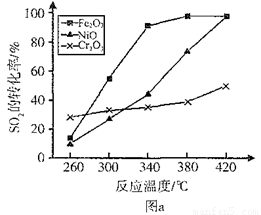
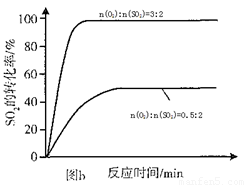
(4)科研小组在3800C Fe2O3作催化剂时,研究了不同投料比n(O2):n(SO2)对S02转化率的影响,结果如图b。请在答题卡坐标图中画出n(O2):n(SO2)=1:2时,SO2转化率的预期变化曲线。
(9分)一定条件下,在一容积可变的密闭容器中,反应: 过程中的能量变化如图所示。反应过程中,A、B、C的物质的量(mol)的变化如下表:
过程中的能量变化如图所示。反应过程中,A、B、C的物质的量(mol)的变化如下表:

|
时间(min) |
0 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
n(A) |
2.00 |
1.90 |
1.82 |
1.76 |
1.64 |
1.54 |
1.50 |
1.50 |
1.50 |
|
n(B) |
1.00 |
0.95 |
0.91 |
0.88 |
0.82 |
0.77 |
0.75 |
0.75 |
0.75 |
|
n(C) |
0 |
0.10 |
0.18 |
0.24 |
0.36 |
0.46 |
0.50 |
0.50 |
0.50 |
回答下列问题:
(1)反应 的正反应△H (填“大于”或“小于”)0。
的正反应△H (填“大于”或“小于”)0。
(2)该反应平衡时,下列说法不正确的是
(A)气体的密度不再改变 (B)A的物质的量浓度不变
(C)放出或吸收的热量不再变化 (D)v正(A)=v逆(A)=0
(3)toC时,在一容积为2L的恒容密闭容器内加入0.4molA和0.6molB,在一定条件下发生反应,反应中C的物质的量浓度变化情况如下图:
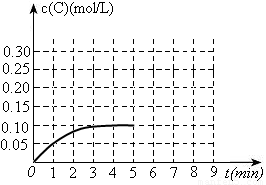
①该温度下,反应: 的平衡常数K=
。
的平衡常数K=
。
②反应进行到1分钟时B物质的量为 。
③在第5min时,将容器的体积缩小一半后,若在第8min达到新的平衡时A的总转化率为75%,请在上图中画出第5min到新平衡时C的物质的量浓度的变化曲线。
(9分)一定条件下,在一容积可变的密闭容器中,反应: 过程中的能量变化如图所示。反应过程中,A、B、C的物质的量(mol)的变化如下表:
过程中的能量变化如图所示。反应过程中,A、B、C的物质的量(mol)的变化如下表:

|
时间(min) |
0 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
n(A) |
2.00 |
1.90 |
1.82 |
1.76 |
1.64 |
1.54 |
1.50 |
1.50 |
1.50 |
|
n(B) |
1.00 |
0.95 |
0.91 |
0.88 |
0.82 |
0.77 |
0.75 |
0.75 |
0.75 |
|
n(C) |
0 |
0.10 |
0.18 |
0.24 |
0.36 |
0.46 |
0.50 |
0.50 |
0.50 |
回答下列问题:
(1)反应 的正反应△H (填“大于”或“小于”)0。
的正反应△H (填“大于”或“小于”)0。
(2)该反应平衡时,下列说法不正确的是
(A)气体的密度不再改变 (B)A的物质的量浓度不变
(C)放出或吸收的热量不再变化 (D)v正(A)=v逆(A)=0
(3)toC时,在一容积为2L的恒容密闭容器内加入0.4molA和0.6molB,在一定条件下发生反应,反应中C的物质的量浓度变化情况如下图:
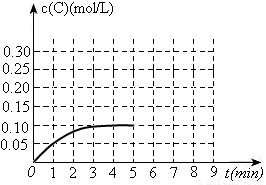
①该温度下,反应: 的平衡常数K=
。
的平衡常数K=
。
②反应进行到1分钟时B物质的量为 。
③在第5min时,将容器的体积缩小一半后,若在第8min达到新的平衡时A的总转化率为75%,请在上图中画出第5min到新平衡时C的物质的量浓度的变化曲线。
 (1)在一定条件下,在一容积可变的密闭容器中,将SO2和O2混合发生反应:
(1)在一定条件下,在一容积可变的密闭容器中,将SO2和O2混合发生反应: