题目内容
 (1)在一定条件下,在一容积可变的密闭容器中,将SO2和O2混合发生反应:
(1)在一定条件下,在一容积可变的密闭容器中,将SO2和O2混合发生反应:2SO2(g)+O2(g)
| 催化剂 |
| △ |
0~4min时,容器气体压强为101KPa.反应过程中,SO2、O2、SO3的物质的量(mol)的变化如下表:
| 时间min | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
| n(SO2) | 2.00 | 1.92 | 1.84 | 1.76 | 1.76 | 1.64 | 1.52 | 1.40 | 1.40 | 1.40 |
| n(O2) | 1.00 | 0.96 | 0.92 | 0.88 | 0.88 | 0.82 | 0.76 | 0.70 | 0.70 | 0.70 |
| n(SO3) | 0 | 0.08 | 0.16 | 0.24 | 0.24 | 0.36 | 0.48 | 0.60 | 0.60 | 0.60 |
①
②第5min时,从速率和转化率两个方面分析,改变的外界条件是
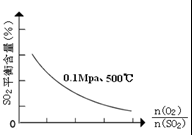
③在0.1Mpa、500℃时,起始时O2和SO2的物质的量之比
| n(O2) |
| n(SO2) |
| n(O2) |
| n(sO2) |
(2)草酸(H2C2O4)是二元弱酸,KHC2O4溶液呈酸性.向10mL 0.01mol?L-1的H2C2O4溶液滴加0.01mol?L-1KOH溶液V(mL),回答下列问题.
①当V<10mL时,反应的离子方程式为
②当V=10mL时,溶液中HC2O4-、C2O42-、H2C2O4、H+的浓度从大到小的顺序为
③当V=amL时,溶液中离子浓度有如下关系:c(K+)=2c(C2O42-)+c(HC2O4-);
当V=bmL时,溶液中离子浓度有如下关系:c(K+)=c(C2O42-)+c(HC2O4-)+c(H2C2O4);则a
④当V=20mL时,再滴入NaOH溶液,则溶液中n(K+)/n(C2O42-)的值将
分析:(1)①依据物质物质的量不变判断反应达到的平衡;
②依据第5min时物质的物质的量变化分析二氧化硫和氧气物质的量减小,三氧化硫物质的量增加,平衡正向进行;
③依据反应是放热反应,降低温度,平衡正向进行,二氧化硫平衡含量随压强和二氧化硫物质的量之比的增大而减小,绘制图象;
(2)草酸(H2C2O4)是二元弱酸,KHC2O4溶液呈酸性.向10mL 0.01mol?L-1的H2C2O4溶液滴加0.01mol?L-1KOH溶液V(mL);
①当V<10mL时,H2C2O4 和KOH反应生成HC2O4 -,还有草酸多余;
②当V=10mL时,H2C2O4 和KOH反应生成KHC2O4 -,KHC2O4溶液呈酸性说明溶液中电离大于水解,比较溶液中HC2O4-、C2O42-、H2C2O4、H+的浓度从大到小的顺序;
③当V=amL时,溶液中离子浓度有如下关系:c(K+)=2c(C2O42-)+c(HC2O4-),依据溶液中电荷守恒分析氢离子浓度和氢氧根离子浓度相同判断;
当V=bmL时,溶液中离子浓度有如下关系:c(K+)=c(C2O42-)+c(HC2O4-)+c(H2C2O4)是溶液中物料守恒分析,溶质为KHC2O4;
④当V=20mL时,反应生成K2C2O4,再滴入NaOH溶液,抑制盐类的水解,n(K+)/n(C2O42-)的值将减小;依据草酸根离子水解平衡影响因素分析判断平衡移动方向;
②依据第5min时物质的物质的量变化分析二氧化硫和氧气物质的量减小,三氧化硫物质的量增加,平衡正向进行;
③依据反应是放热反应,降低温度,平衡正向进行,二氧化硫平衡含量随压强和二氧化硫物质的量之比的增大而减小,绘制图象;
(2)草酸(H2C2O4)是二元弱酸,KHC2O4溶液呈酸性.向10mL 0.01mol?L-1的H2C2O4溶液滴加0.01mol?L-1KOH溶液V(mL);
①当V<10mL时,H2C2O4 和KOH反应生成HC2O4 -,还有草酸多余;
②当V=10mL时,H2C2O4 和KOH反应生成KHC2O4 -,KHC2O4溶液呈酸性说明溶液中电离大于水解,比较溶液中HC2O4-、C2O42-、H2C2O4、H+的浓度从大到小的顺序;
③当V=amL时,溶液中离子浓度有如下关系:c(K+)=2c(C2O42-)+c(HC2O4-),依据溶液中电荷守恒分析氢离子浓度和氢氧根离子浓度相同判断;
当V=bmL时,溶液中离子浓度有如下关系:c(K+)=c(C2O42-)+c(HC2O4-)+c(H2C2O4)是溶液中物料守恒分析,溶质为KHC2O4;
④当V=20mL时,反应生成K2C2O4,再滴入NaOH溶液,抑制盐类的水解,n(K+)/n(C2O42-)的值将减小;依据草酸根离子水解平衡影响因素分析判断平衡移动方向;
解答:解:(1)①图表数据分析可知在3~4min和7~9min时,二氧化硫、氧气和三氧化硫物质的量不变说明反应达到平衡;
故答案为:3~4min和7~9min;
②第5min时物质的物质的量变化分析二氧化硫和氧气物质的量减小,三氧化硫物质的量增加,平衡正向进行,依据平衡移动原理分析可知增大压强平衡正向进行;符合物质的量变化;
故答案为:增大压强;正;
③反应是放热反应,降低温度,平衡正向进行,二氧化硫含量比500°C时小,二氧化硫平衡含量随氧气和二氧化硫物质的量之比的增大而减小,绘制图象为;
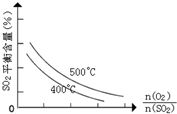
故答案为:
 ;
;
(2)①当V<10mL时,H2C2O4 和KOH反应生成HC2O4 -,还有草酸多余,反应的离子方程式为:H2C2O4+OH-=HC2O4-+H2O;
故答案为:H2C2O4+OH-=HC2O4-+H2O;
②当V=10mL时,H2C2O4 和KOH反应生成KHC2O4 -,KHC2O4溶液呈酸性说明溶液中电离大于水解,比较溶液中HC2O4-、C2O42-、H2C2O4、H+的浓度从大到小的顺序为:c(HC2O4-)>c(H+)>c(C2O42-)>c(H2C2O4);
故答案为:c(HC2O4-)>c(H+)>c(C2O42-)>c(H2C2O4);
③当V=amL时,溶液中离子浓度有如下关系:c(K+)=2c(C2O42-)+c(HC2O4-),依据溶液中电荷守恒分析氢离子浓度和氢氧根离子浓度相同判断,溶液中溶质为KHC2O4;和为K2C2O4 ;
当V=bmL时,溶液中离子浓度有如下关系:c(K+)=c(C2O42-)+c(HC2O4-)+c(H2C2O4)是溶液中物料守恒分析,溶质为KHC2O4;说明a大于b;
故答案为:>;
④当V=20mL时,反应生成K2C2O4,再滴入NaOH溶液,抑制盐类的水解,n(K+)/n(C2O42-)的值将减小;因为溶液中存在如下平衡C2O42-+H2O?HC2O4-+OH-,当增大c(OH-)时,平衡向逆方向移动,n(C2O42-)的值变大,而n(K+)的值不变,故n(K+)/n(C2O42-)的值变小;
故答案为:变小,因为溶液中存在如下平衡C2O42-+H2O?HC2O4-+OH-,当增大c(OH-)时,平衡向逆方向移动,n(C2O42-)的值变大,而n(K+)的值不变,故n(K+)/n(C2O42-)的值变小;
故答案为:3~4min和7~9min;
②第5min时物质的物质的量变化分析二氧化硫和氧气物质的量减小,三氧化硫物质的量增加,平衡正向进行,依据平衡移动原理分析可知增大压强平衡正向进行;符合物质的量变化;
故答案为:增大压强;正;
③反应是放热反应,降低温度,平衡正向进行,二氧化硫含量比500°C时小,二氧化硫平衡含量随氧气和二氧化硫物质的量之比的增大而减小,绘制图象为;

故答案为:
 ;
;(2)①当V<10mL时,H2C2O4 和KOH反应生成HC2O4 -,还有草酸多余,反应的离子方程式为:H2C2O4+OH-=HC2O4-+H2O;
故答案为:H2C2O4+OH-=HC2O4-+H2O;
②当V=10mL时,H2C2O4 和KOH反应生成KHC2O4 -,KHC2O4溶液呈酸性说明溶液中电离大于水解,比较溶液中HC2O4-、C2O42-、H2C2O4、H+的浓度从大到小的顺序为:c(HC2O4-)>c(H+)>c(C2O42-)>c(H2C2O4);
故答案为:c(HC2O4-)>c(H+)>c(C2O42-)>c(H2C2O4);
③当V=amL时,溶液中离子浓度有如下关系:c(K+)=2c(C2O42-)+c(HC2O4-),依据溶液中电荷守恒分析氢离子浓度和氢氧根离子浓度相同判断,溶液中溶质为KHC2O4;和为K2C2O4 ;
当V=bmL时,溶液中离子浓度有如下关系:c(K+)=c(C2O42-)+c(HC2O4-)+c(H2C2O4)是溶液中物料守恒分析,溶质为KHC2O4;说明a大于b;
故答案为:>;
④当V=20mL时,反应生成K2C2O4,再滴入NaOH溶液,抑制盐类的水解,n(K+)/n(C2O42-)的值将减小;因为溶液中存在如下平衡C2O42-+H2O?HC2O4-+OH-,当增大c(OH-)时,平衡向逆方向移动,n(C2O42-)的值变大,而n(K+)的值不变,故n(K+)/n(C2O42-)的值变小;
故答案为:变小,因为溶液中存在如下平衡C2O42-+H2O?HC2O4-+OH-,当增大c(OH-)时,平衡向逆方向移动,n(C2O42-)的值变大,而n(K+)的值不变,故n(K+)/n(C2O42-)的值变小;
点评:本题考查了化学平衡的建立过程分析,溶液中离子浓度大小比较方法,量不同酸碱反应生成的产物不同,掌握基础是关键,题目难度较大.

练习册系列答案
相关题目