ЬтФПФкШн
A~FСљжжгаЛњЮяЕФЯрЛЅзЊЛЏЙиЯЕШчЭМЫљЪОЃК
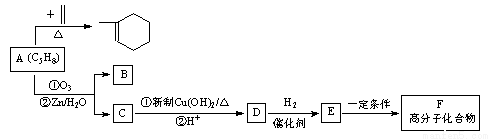
вбжЊ ЃК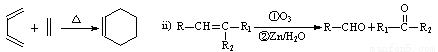
ОнДЫЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉAЪЧКЯГЩЬьШЛЯ№НКЕФЕЅЬхЃЌгУЯЕЭГУќУћЗЈУќУћЃЌAЕФУћГЦЮЊ ЃЌЬьШЛЯ№НКЕФНсЙЙМђЪНЮЊ _ЁЃ
ЃЈ2ЃЉAЩњГЩ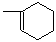 ЪБЃЌAЗЂЩњЕФЗДгІРраЭЮЊ ЁЃ
ЪБЃЌAЗЂЩњЕФЗДгІРраЭЮЊ ЁЃ
ЃЈ3ЃЉEЁњFЕФЛЏбЇЗНГЬЪНЮЊ ЁЃ
ЃЈ4ЃЉAгыBr2АДЮяжЪЕФСПБШ1ЁУ1ЗЂЩњМгГЩЗДгІЃЌЩњГЩЕФВњЮяга _жж(ПМТЧЫГЗДвьЙЙ)ЁЃ
ЃЈ5ЃЉЯжгаСэвЛжжгаЛњЮяGЃЌвбжЊGгыEЮоТлАДКЮжжБШР§ЛьКЯЃЌжЛвЊзмжЪСПвЛЖЈЃЌЭъШЋШМЩеЪБЩњГЩЕФCO2ЁЂH2OвдМАЯћКФЕФO2ОљЮЊЖЈжЕЁЃЧыаДГіСНжжЗћКЯЯТСавЊЧѓЕФGЕФНсЙЙМђЪН _ЁЂ ЁЃ
ЂйM(G)ЃМM(E)ЃЛ
ЂкGЕФКЫДХЙВеёЧтЦзБэУїЦфгаСНжжВЛЭЌЛЏбЇЛЗОГЕФЧтЃЌЧвЗхУцЛ§БШЮЊ1ЁУ3ЁЃ
ЃЈ1ЃЉ2ЃМзЛљЃ1ЃЌ3ЃЖЁЖўЯЉЃЈ2ЗжЃЉЃЛ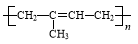 ЃЈ2ЗжЃЉ
ЃЈ2ЗжЃЉ
ЃЈ2ЃЉ1ЃЌ4ЃМгГЩЗДгІ(1Зж)
ЃЈ3ЃЉ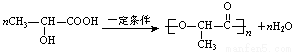 ЃЈ2ЗжЃЉ
ЃЈ2ЗжЃЉ
Лђ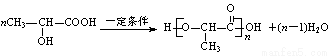
ЃЈ4ЃЉ4 ЃЈ2ЗжЃЉ
ЃЈ5ЃЉCH3COOHЃЛHCOOCH3(4Зж) )
ЁОНтЮіЁП
ЪдЬтЗжЮіЃКЃЈ1ЃЉгЩAгыввЯЉМгГЩЕФВњЮяХаЖЯAЮЊвьЮьЖўЯЉЃЌЯЕЭГУќУћЗЈЪЧ2ЃМзЛљЃ1ЃЌ3ЃЖЁЖўЯЉЃЛЗЂЩњМгОлЗДгІЕУЬьШЛЯ№НКЃЌЦфНсЙЙМђЪНЮЊ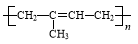
ЃЈ2ЃЉAгыввЯЉЗЂЩњ1ЃЌ4ЃМгГЩЗДгІЩњГЩ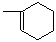
ЃЈ3ЃЉгЩвбжЊЕУAЗЂЩњЗДгІЩњГЩBЁЂCЃЌBЮЊМзШЉЃЌCЗжзгжаКЌгаШЉЛљЁЂєЪЛљЃЌЫљвдEЮЊІС-єЧЛљБћЫсЃЌдђEЁњFЕФЛЏбЇЗНГЬЪНЮЊ
ЃЈ4ЃЉAгыBr2АДЮяжЪЕФСПБШ1ЁУ1ЗЂЩњМгГЩЗДгІЃЌМгГЩЗНЪНга2жжЃК1,2МгГЩЃЌ1,4МгГЩЃЌЕУЕН3жжВњЮяЃЌЦфжа1,4МгГЩЕФВњЮяДцдкЫГЗДвьЙЙЃЌЫљвдЙВ4жжЁЃ
ЃЈ5ЃЉGгыEЮоТлАДКЮжжБШР§ЛьКЯЃЌжЛвЊзмжЪСПвЛЖЈЃЌЭъШЋШМЩеЪБЩњГЩЕФCO2ЁЂH2OвдМАЯћКФЕФO2ОљЮЊЖЈжЕЃЌЫЕУїGгыEЕФЪЕбщЪНЯрЭЌЃЌЮЊCH2OЃЌгжM(G)ЃМM(E)ЃЌGЕФКЫДХЙВеёЧтЦзБэУїЦфгаСНжжВЛЭЌЛЏбЇЛЗОГЕФЧтЃЌЧвЗхУцЛ§БШЮЊ1ЁУ3ЃЌЫЕУїGжага4ИіЧтдзгЃЌСНжжЕШаЇЧтЃЌЫљвдGЕФЗжзгЪНЮЊC2H4O2ЃЌЦфНсЙЙМђЪНЮЊCH3COOHЁЂHCOOCH3
ПМЕуЃКПМВщгаЛњЮяЕФЭЦЖЯЃЌЖўЯЉЬўЕФМгГЩЗДгІВњЮяЕФХаЖЯЃЌНсЙЙМђЪНЕФЭЦЖЯЃЌЛЏбЇЗНГЬЪНЕФЪщаД

 УћЪІжИЕМЦкФЉГхДЬОэЯЕСаД№АИ
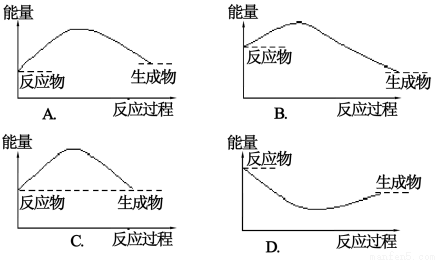
УћЪІжИЕМЦкФЉГхДЬОэЯЕСаД№АИЕЊЪЧЕиЧђЩЯКЌСПЗсИЛЕФвЛжждЊЫиЃЌЕЊМАЦфЛЏКЯЮядкЙЄХЉвЕЩњВњЁЂЩњЛюжагазХживЊзїгУЃЌМѕЩйЕЊЕФбѕЛЏЮядкДѓЦјжаЕФХХЗХЪЧЛЗОГБЃЛЄЕФживЊФкШнжЎвЛЁЃ
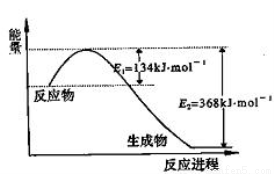
ЃЈ1ЃЉЩЯЭМЪЧ1 mol NO2ЦјЬхКЭ1 mol COЦјЬхЗДгІЩњГЩCO2ЦјЬхКЭNOЦјЬхЙ§ГЬжаФмСПБфЛЏЪОвтЭМЃЌЧыаДГіNO2КЭCOЗДгІЕФШШЛЏбЇЗНГЬЪНЃК ЃЛ
вбжЊЃКN2 (g)+2NO2 (g)  4NO(g) ЁїH=+292.3kJЁЄmolЁЊ1ЃЌ
4NO(g) ЁїH=+292.3kJЁЄmolЁЊ1ЃЌ
дђЗДгІЃК 2NO(g)+2CO(g) N2(g)+2CO2(g) ЕФЁїH= ЃЛ
N2(g)+2CO2(g) ЕФЁїH= ЃЛ
ЃЈ2ЃЉвЛЖЈЮТЖШЯТЃЌдкЬхЛ§ЮЊ2LЕФКуШнУмБеШнЦїжаГфШы20 mol NO2КЭ5 mol O2ЗЂЩњЗДгІЃК 4NO2(g)+O2(g) 2N2O5(g)ЃЛвбжЊЬхЯЕжаn(NO2)ЫцЪБМфБфЛЏШчЯТБэЃК
2N2O5(g)ЃЛвбжЊЬхЯЕжаn(NO2)ЫцЪБМфБфЛЏШчЯТБэЃК
t(s) | 0 | 500 | 1000 | 1500 |
n(NO2)(mol) | 20 | 13.96 | 10.08 | 10.08 |
ЂйаДГіИУЗДгІЕФЦНКтГЃЪ§БэДяЪНЃКK= ЃЌвбжЊЃКK3000CЃОK3500CЃЌдђИУЗДгІЪЧ ЗДгІ(ЬюЁАЗХШШЁБЛђЁАЮќШШЁБ)ЃЛ
ЂкЗДгІДяЕНЦНКтКѓЃЌNO2ЕФзЊЛЏТЪЮЊ ЃЌШєвЊдіДѓNO2ЕФзЊЛЏТЪЃЌПЩВЩШЁЕФДыЪЉга
AЃЎНЕЕЭЮТЖШ
BЃЎГфШыКЄЦјЃЌЪЙЬхЯЕбЙЧПдіДѓ
CЃЎдйГфШыNO2
DЃЎдйГфШы4 mol NO2КЭ1 mol O2
ЂлЭМжаБэЪОN2O5ЕФХЈЖШЕФБфЛЏЧњЯпЪЧ ЃЌгУO2БэЪОДг0~500sФкИУЗДгІЕФЦНОљЫйТЪv= ЁЃ

гУ0.1320 mol/LЕФHClШмвКЕЮЖЈЮДжЊХЈЖШЕФNaOHШмвКЃЌЪЕбщЪ§ОнШчЯТБэЫљЪОЃЌ
ЪЕбщБрКХ | Д§ВтNaOHШмвКЕФЬхЛ§/mL | HClШмвКЕФЬхЛ§/mL |
1 | 25.00 | 24.41 |
2 | 25.00 | 24.39 |
3 | 25.00 | 22.60 |
ЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉЭМжаМзЮЊ ЕЮЖЈЙмЃЌввЮЊ ЕЮЖЈЙмЃЈЬюЁАЫсЪНЁБЛђЁАМюЪН ЁБЃЉЃЛ
ЃЈ2ЃЉШЁД§ВтвКNaOHШмвК25.00 mL гкзЖаЮЦПжаЃЌЪЙгУ зіжИЪОМСЃЌЕЮЖЈжеЕуЕФХаЖЯвРОнЪЧ ЃЛ
ЃЈ3ЃЉШєЕЮЖЈЧАЃЌЕЮЖЈЙмМтЖЫгаЦјХнЃЌЕЮЖЈКѓЦјХнЯћЪЇЃЌНЋЪЙЫљВтНсЙћ ЃЈЬюЁАЦЋИпЁБЁЂЁАЦЋЕЭЁБЛђЁАВЛБфЁБЃЌЯТЭЌЃЉЃЌШєЖСЫсЪНЕЮЖЈЙмЖСЪ§ЪБЃЌЕЮЖЈЧАбіЪгЖСЪ§ЃЌЕЮЖЈКѓе§ШЗЖСЪ§ЃЌдђЫљВтНсЙћ ЃЛ
ЃЈ4ЃЉИУNaOHШмвКЕФЮяжЪЕФСПХЈЖШЮЊ mol/L (БЃСєаЁЪ§ЕуКѓЫФЮЛгааЇЪ§зж)ЁЃ