题目内容
【题目】在标准状况下,4.48L的NH3气体物质的量为mol质量为g,其中含个氢原子,将其溶于水配成200mL的溶液,其物质的量浓度为mol/L.
【答案】0.2;3.4;0.6;1
【解析】解:标准状况下4.48L的NH3的物质的量为: ![]() =0.2 mol,质量为:m=nM=0.2 mol×17 g/mol=3.4 g;0.2mol氨气分子中含有H原子的物质的量为:0.2mol×3=0.6mol,含有氢原子数为0.6NA , 将0.2mol氨气溶于水配成200mL溶液,所得溶液的物质的量浓度为:c=
=0.2 mol,质量为:m=nM=0.2 mol×17 g/mol=3.4 g;0.2mol氨气分子中含有H原子的物质的量为:0.2mol×3=0.6mol,含有氢原子数为0.6NA , 将0.2mol氨气溶于水配成200mL溶液,所得溶液的物质的量浓度为:c= ![]() =
= ![]() =1 mol/L.故答案为:0.2;3.4;0.6NA;1.
=1 mol/L.故答案为:0.2;3.4;0.6NA;1.
根据n= ![]() 计算出标准状况下4.48L氨气的物质的量,然后根据m=nM计算出氨气的质量;氨气分子中含有3个H原子,根据氨气的物质的量计算出含有H原子的物质的量;最后根据c=
计算出标准状况下4.48L氨气的物质的量,然后根据m=nM计算出氨气的质量;氨气分子中含有3个H原子,根据氨气的物质的量计算出含有H原子的物质的量;最后根据c= ![]() 计算出所得溶液的物质的量浓度.
计算出所得溶液的物质的量浓度.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
【题目】如图是制取、净化并测量生成气体体积的装置示图。利用如图装置进行下表所列实验,能达到实验目的的是
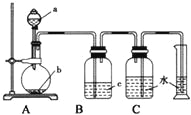
选项 | a(液体) | b(固体) | c(液体) |
A | 饱和食盐水 | 电石 | 硫酸铜溶液 |
B | 浓氨水 | 生石灰 | 浓硫酸 |
C | 稀硫酸 | 硫化亚铁 | 浓硫酸 |
D | 浓硫酸 | Cu片 | 氢氧化钠溶液 |
A. A B. B C. C D. D