题目内容
如图中的实线表示元素周期表的部分边界.①~⑥分别表示元素周期表中对应位置的元素.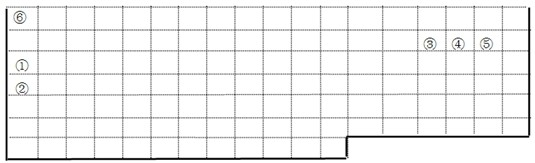
(1)请在图中用实线补全元素周期表边界.
(2)元素⑤的原子核外p电子数比s电子总数多______个,元素⑤的原子结构示意图为______.
(3)由元素④和⑥组成的化合物的稀溶液中加入少量二氧化锰粉末,有无色气体生成.则该反应的化学方程式为______.
(4)已知甲元素位于第3周期,且其原子半径为同周期金属元素中原子半径最小的,请写出甲的氧化物与NaOH溶液反应的离子方程式______;在一定条件下1g⑥的单质在足量④的单质中完全燃烧生成液态物质时,放出的热量为a kJ,请写出此条件下表示⑥的单质燃烧热的热化学方程式______.

(1)请在图中用实线补全元素周期表边界.
(2)元素⑤的原子核外p电子数比s电子总数多______个,元素⑤的原子结构示意图为______.
(3)由元素④和⑥组成的化合物的稀溶液中加入少量二氧化锰粉末,有无色气体生成.则该反应的化学方程式为______.
(4)已知甲元素位于第3周期,且其原子半径为同周期金属元素中原子半径最小的,请写出甲的氧化物与NaOH溶液反应的离子方程式______;在一定条件下1g⑥的单质在足量④的单质中完全燃烧生成液态物质时,放出的热量为a kJ,请写出此条件下表示⑥的单质燃烧热的热化学方程式______.
根据元素周期表的结构和元素的分布,可推知:①为Na,②为K,③为N,④为O,⑤为F,⑥为H.
(1)元素周期表的结构以及元素的分布情况,表示元素周期表的部分边界如下: ,
,
故答案为: ;
;
(2)F原子含有9个质子,核外电子排布式为:1s22s22p5,p电子数为5个,s电子数为2+2=4个,因此p电子数比s电子总数多1个;F原子结构示意图为: ,故答案为:1;
,故答案为:1; ;
;
(3)由O和H组成的化合物中过氧化氢的稀溶液中加入少量二氧化锰粉末,有氧气生成,化学方程式为:2H2O2
2H2O+O2↑,
故答案为:2H2O2
2H2O+O2↑;
(4)第三周期金属原子半径最小的为Al,其氧化物氧化铝与氢氧化钠反应生成偏铝酸钠和水,离子方程式为:Al2O3+2OH-=2AlO2-+H2O;1g氢气的物质的量为0.5mol,则1mol氢气氧气中完全燃烧生成液态水,放出热量2akJ,氢气燃烧热的热化学方程式为:H2(g)+
O2(g)=H2O(l)△H=-2aKJ/mol,
故答案为:Al2O3+2OH-=2AlO2-+H2O;H2(g)+
O2(g)=H2O(l)△H=-2aKJ/mol.
(1)元素周期表的结构以及元素的分布情况,表示元素周期表的部分边界如下:
 ,
,故答案为:
 ;
;(2)F原子含有9个质子,核外电子排布式为:1s22s22p5,p电子数为5个,s电子数为2+2=4个,因此p电子数比s电子总数多1个;F原子结构示意图为:
 ,故答案为:1;
,故答案为:1; ;
;(3)由O和H组成的化合物中过氧化氢的稀溶液中加入少量二氧化锰粉末,有氧气生成,化学方程式为:2H2O2
| ||
故答案为:2H2O2
| ||
(4)第三周期金属原子半径最小的为Al,其氧化物氧化铝与氢氧化钠反应生成偏铝酸钠和水,离子方程式为:Al2O3+2OH-=2AlO2-+H2O;1g氢气的物质的量为0.5mol,则1mol氢气氧气中完全燃烧生成液态水,放出热量2akJ,氢气燃烧热的热化学方程式为:H2(g)+
| 1 |
| 2 |
故答案为:Al2O3+2OH-=2AlO2-+H2O;H2(g)+
| 1 |
| 2 |

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目