题目内容
【题目】据《天工开物》记载,我国古代以炉甘石(主要成分是ZnCO3)来冶炼倭铅(即锌),其原理如图2。已知锌的熔点420℃、沸点906℃。则下列说法错误的是( )

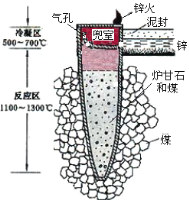
图1 图2
A.“泥封”的目的是为了防止得到的锌被氧化
B.“锌火”是锌蒸气和一氧化碳在空气的燃烧
C.冶炼时锌变为蒸气在兜室冷凝为固体
D.升炼倭铅过程包含分解反应和氧化还原反应
【答案】C
【解析】A、锌是活泼金属,泥封隔绝空气,防止锌被氧化,故说法正确;B、煤在氧气不足时产生CO,根据反应区的温度,锌为蒸气,因此锌火是锌蒸气和CO在空气燃烧,故说法正确;C、兜室的温度高于锌的熔点,此时锌为液体,故说法正确;D、ZnCO3受热分解,用CO还原ZnO得到Zn,属于氧化还原反应,故说法正确。

练习册系列答案
相关题目
