题目内容
5.化学中常用图象直观地描述化学反应的进程或结果.下列图象描述正确的是( )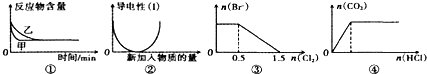
| A. | 图①标上压强可对逆反应2A(g)+2B(g)?3C(g)+D(g)的影响,乙的压强大 | |
| B. | 图②表示向乙酸溶液中通入氨气至过量的过程,溶液导电性变化 | |
| C. | 图③表示在1L1mol/LFeBr2溶液中通入Cl2时Br-的量的变化 | |
| D. | 图④表示一定浓度Na2CO3溶液中逐滴滴加盐酸与生成CO2的物质的量的关系 |
分析 A.该反应是反应前后气体体积不变的可逆反应,增大压强平衡不移动,则物质的转化率不变,压强移动,反应速率越大,反应达到平衡的时间越短;
B.溶液中离子浓度越大溶液的导电性越强;
C.向溴化亚铁中通入氯气时,先氧化亚铁离子后氧化溴离子,溴化铁溶液中c(Fe2+):c(Br-)=1:2,反应方程式为2Fe2++Cl2=2Cl-+2Fe3+、2Br-+Cl2=Br2+2Cl-,根据方程式知,第一段消耗氯气为第二段的一半;
D.向碳酸钠溶液中逐滴滴加HCl时发生的反应为Na2CO3+HCl=NaCl+NaHCO3、NaHCO3+HCl=NaCl+H2O+CO2↑,根据反应方程式判断生成气体与加入HCl的关系.
解答 解:A.该反应是反应前后气体体积不变的可逆反应,增大压强平衡不移动,则物质的转化率不变,压强移动,反应速率越大,反应达到平衡的时间越短,根据到达平衡的时间判断,甲的压强大于乙,故A错误;
B.溶液中离子浓度越大溶液的导电性越强,向乙酸溶液中通入氨气至过量的过程,乙酸和一水合氨都是弱电解质、醋酸铵是强电解质,随着氨气的通入,溶液中离子浓度增大溶液导电性增大,故B错误;
C.向溴化亚铁中通入氯气时,先氧化亚铁离子后氧化溴离子,溴化铁溶液中c(Fe2+):c(Br-)=1:2,反应方程式为2Fe2++Cl2=2Cl-+2Fe3+、2Br-+Cl2=Br2+2Cl-,根据方程式知,第一段消耗氯气为第二段的一半,故C正确;
D.向碳酸钠溶液中逐滴滴加HCl时发生的反应为Na2CO3+HCl=NaCl+NaHCO3、NaHCO3+HCl=NaCl+H2O+CO2↑,根据反应方程式知,先没有气体生成当碳酸钠完全转化为碳酸氢钠后再滴加稀盐酸有气体生成,故D错误;
故选C.
点评 本题考查化学反应速率的影响因素及化学平衡影响因素、氧化还原反应的计算、方程式的计算、电解质溶液导电性等知识点,综合性较强,明确物质的性质及离子反应先后顺序等知识点即可解答,易错选项是C.

| A. | 食品添加剂对人体的健康均无害,所以不用严格控制用量 | |
| B. | 棉、麻、丝、毛的主要成分都是纤维素 | |
| C. | 光纤的主要成分是二氧化硅 | |
| D. | 农业施肥所用的碳铵和尿素均属于无机物 |
| A. | 肯定有Al3+、Mg2+、Cl-,可能有NH4+ | |
| B. | 肯定有Al3+、Mg2+、HCO3-,肯定没有MnO4- | |
| C. | 肯定有K+、Al3+、MnO4-,可能有HCO3- | |
| D. | 肯定有Al3+、Mg2+、Cl-,可能有K+ |
| A. | 原子核外每层最多容纳的电子数为2n2个(n为电子层) | |
| B. | 同一原子核外的M层上的电子数一定比L层上的电子数多 | |
| C. | 如果原子只有一个电子层,该原子的质子数不超过2个 | |
| D. | 1~18号元素,每层电子数都满足2n2个电子的元素只有2种 |
| A. | ①②③④ | B. | ④⑤⑥ | C. | ②④⑥ | D. | ②③⑤ |
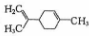 ,有关柠檬烯的分析正确的是( )
,有关柠檬烯的分析正确的是( )| A. | 一氯代物共有7种 | |
| B. | 分子中所有碳原子一定在同一平面 | |
| C. | 和丁基苯(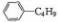 )互为同分异构体 )互为同分异构体 | |
| D. | 一定条件下,分别可以发生加成、取代、氧化反应 |
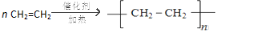 .
.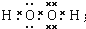 ;将乙加入浅绿色酸性溶液中,溶液变为棕黄色,写出该反应的离子方程式.
;将乙加入浅绿色酸性溶液中,溶液变为棕黄色,写出该反应的离子方程式. .与PH3相比,DC2易液化的主要原因是NH3中有氢键;
.与PH3相比,DC2易液化的主要原因是NH3中有氢键;