题目内容
(7分)回答问题:
(1)甲、乙两试管分别盛有5 mLFeCl3溶液和5 mLFeCl2溶液,各滴入几滴KSCN溶液。填写下表:
(2)在盛有3 mLFeCl3溶液的试管中加入少量铁粉,若充分反应后没有固体物剩余。该试管的溶液中存在什么金属阳离子?如何进一步得到肯定答案?
(1)甲、乙两试管分别盛有5 mLFeCl3溶液和5 mLFeCl2溶液,各滴入几滴KSCN溶液。填写下表:
| 试 样 | 滴入KSCN溶液后的现象 | 两试管里产生不同的现象有何用途 |
| 甲试管(FeCl3) | | |
| 乙试管(FeCl2) | |
(1)溶液变成红色;溶液没有变色;常用KSCN溶液检验Fe3+的存在。(3分)
(2)答:若铁粉不足,反应后溶液里存在的金属离子可能是Fe2+和Fe3+,若铁粉恰好与Fe3+完全反应,则反应后溶液中的金属离子是Fe2+。(2分)
取少量反应后的溶液于另一试管中,滴入几滴KSCN溶液,观察溶液是否变红,若变红说明是Fe2+和Fe3+,若不变色,则说明是Fe2+。(2分)
(2)答:若铁粉不足,反应后溶液里存在的金属离子可能是Fe2+和Fe3+,若铁粉恰好与Fe3+完全反应,则反应后溶液中的金属离子是Fe2+。(2分)
取少量反应后的溶液于另一试管中,滴入几滴KSCN溶液,观察溶液是否变红,若变红说明是Fe2+和Fe3+,若不变色,则说明是Fe2+。(2分)
略

练习册系列答案
相关题目
 重要的地位,了解铁及其化合物的性质和用途非常重要。请回答下列问题:
重要的地位,了解铁及其化合物的性质和用途非常重要。请回答下列问题: 加入试液,滴入KSCN溶液,若显血红色,证明一定存在Fe3+。
加入试液,滴入KSCN溶液,若显血红色,证明一定存在Fe3+。
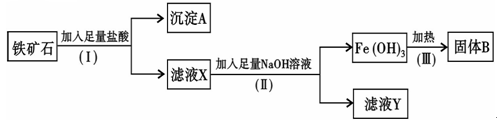
 (填化学式),固体B是 (填化学式);
(填化学式),固体B是 (填化学式);