题目内容
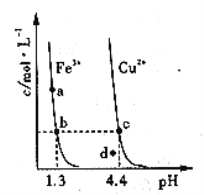
【题目】图1是铜锌原电池示意图.图2中,x轴表示实验时流入正极的电子的物质的量,y轴表示( ) 
A.铜棒的质量
B.c(Zn2+)
C.c(H+)
D.c(SO42﹣)
【答案】C
【解析】解:铜锌原电池中,Zn是负极,失去电子发生氧化反应,电极反应为Zn﹣2e﹣=Zn2+ , Cu是正极,氢离子得电子发生还原反应,电极反应为 2H++2e﹣=H2↑, A.Cu是正极,氢离子得电子发生还原反应,Cu棒的质量不变,故A错误;
B.由于Zn是负极,不断发生反应Zn﹣2e﹣=Zn2+ , 所以溶液中c(Zn2+)增大,故B错误;
C.由于反应不断消耗H+ , 所以溶液的c(H+)逐渐降低,故C正确;
D.SO42﹣不参加反应,其浓度不变,故D错误;
故选:C.
铜锌原电池中,Zn是负极,失去电子发生氧化反应,电极反应为Zn﹣2e﹣=Zn2+ , Cu是正极,氢离子得电子发生还原反应,电极反应为2H++2e﹣=H2↑,据此解答.

练习册系列答案
相关题目