题目内容
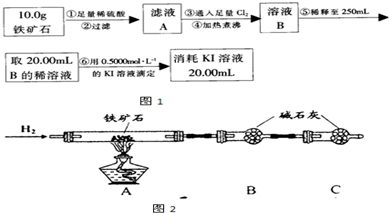
铁矿石是工业炼铁的主要原料之一,其主要成分为铁的氧化物(设杂质中不含铁元素和氧元素,且杂质不与H2SPO4反应).某研究性学习小组对某铁矿石中铁的氧化物的化学式进行探究.

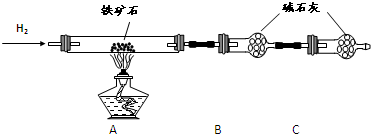
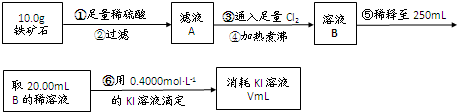
Ⅰ.铁矿石中含氧量的测定
①按如图组装仪器,检查装置的气密性;
②将5.0g铁矿石放入硬质玻璃管中,装置B、C中的药品如图所示(夹持仪器均省略):
③从左端导气管口处不断地缓缓通入H2,待C装置出口处H2验纯后,点燃A处酒精灯;
④充分反应后,撤掉酒精灯,再持续通入氢气至完全冷却.
(1)装置C的作用为 .
(2)测得反应后装置B增重1.35g,则铁矿石中氧的百分含量为 .
(3)若将H2换成CO,则还需补充 装置.
Ⅱ.铁矿石中含铁量的测定
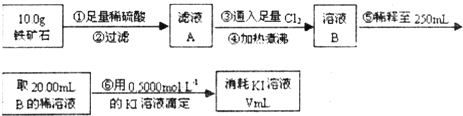
(4)步骤④中煮沸的作用是 .
(5)步骤⑤中用到的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还有 .
(6)下列有关步骤⑥的操作中说法正确的是 .
a.因为碘水为黄色,所以滴定过程中不需加指示剂
b.滴定过程中可利用淀粉溶液作为指示剂
c.滴定管用蒸馏水洗涤后可以直接装液
d.锥形瓶不需要用待测液润洗
e.滴定过程中,眼睛注视滴定管中液面变化
f.滴定结束后,30s内溶液不恢复原来的颜色,再读数
(7)若滴定过程中消耗0.5000mol?L-1的KI溶液20.00mL,则铁矿石中铁的百分含量为 .
Ⅲ.(8)由I、II可以推算出该铁矿石中铁的氧化物的化学式 .

Ⅰ.铁矿石中含氧量的测定
①按如图组装仪器,检查装置的气密性;
②将5.0g铁矿石放入硬质玻璃管中,装置B、C中的药品如图所示(夹持仪器均省略):
③从左端导气管口处不断地缓缓通入H2,待C装置出口处H2验纯后,点燃A处酒精灯;
④充分反应后,撤掉酒精灯,再持续通入氢气至完全冷却.
(1)装置C的作用为
(2)测得反应后装置B增重1.35g,则铁矿石中氧的百分含量为
(3)若将H2换成CO,则还需补充
Ⅱ.铁矿石中含铁量的测定

(4)步骤④中煮沸的作用是
(5)步骤⑤中用到的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还有
(6)下列有关步骤⑥的操作中说法正确的是
a.因为碘水为黄色,所以滴定过程中不需加指示剂
b.滴定过程中可利用淀粉溶液作为指示剂
c.滴定管用蒸馏水洗涤后可以直接装液
d.锥形瓶不需要用待测液润洗
e.滴定过程中,眼睛注视滴定管中液面变化
f.滴定结束后,30s内溶液不恢复原来的颜色,再读数
(7)若滴定过程中消耗0.5000mol?L-1的KI溶液20.00mL,则铁矿石中铁的百分含量为
Ⅲ.(8)由I、II可以推算出该铁矿石中铁的氧化物的化学式
分析:(1)B中的碱石灰是吸收置换反应生成的水的,为了防止空气成分对实验的影响,要加一个装置吸收空气中的水以及二氧化碳;
(2)反应后装置B增重1.35g,即氢气和氧化铁反应后固体质量的增加值,可以根据差量法来计算;
(3)若将H2换成CO,CO有毒,不能排入空气中;
(4)煮沸可以排除水中的氯气,防止实验误差;
(5)根据稀释液体和配制一定体积的溶液所选择的仪器来回答;
(6)根据滴定实验以及滴定过程中的实验误差分析知识判断;
(7)根据元素守恒和化学反应方程式进行计算;
(8)根据铁元素质量分数和氧元素质量分数计算出铁的氧化物的化学式.
(2)反应后装置B增重1.35g,即氢气和氧化铁反应后固体质量的增加值,可以根据差量法来计算;
(3)若将H2换成CO,CO有毒,不能排入空气中;
(4)煮沸可以排除水中的氯气,防止实验误差;
(5)根据稀释液体和配制一定体积的溶液所选择的仪器来回答;
(6)根据滴定实验以及滴定过程中的实验误差分析知识判断;
(7)根据元素守恒和化学反应方程式进行计算;
(8)根据铁元素质量分数和氧元素质量分数计算出铁的氧化物的化学式.
解答:解:Ⅰ.(1)该实验中,氢气和氧化铁反应生成金属铁和水,根据固体质量的变化来计算铁的含量,B处的干燥管作用是吸收产生的水蒸气,所以C装置要防止防止空气中的水蒸气和CO2进入B中,影响测定结果,
故答案为:防止空气中的水蒸气和CO2进入B中,影响测定结果;
(2)测的反应后装置B增重1.35g,根据反应的实质,增加的是氧元素的质量,所以氧元素的质量分数是:
×100%=24%,
故答案为:24%;
(3)因CO有毒,不能排放到空气中,应加尾气处理装置,故答案为:尾气处理;
Ⅱ.(4)向铁矿石中加入硫酸,酸化反应生成硫酸的铁盐溶液,还存在过量的硫酸溶液,加入过量的氯气,煮沸的作用是赶走溶液中溶解的过量的Cl2,否则会影响与KI的反应,带来实验误差,
故答案为:赶走溶液中溶解的过量的Cl2;
(5)若稀释到250mL,采用的仪器有:烧杯、玻璃棒、胶头滴管、250mL容量瓶,故答案为:250mL容量瓶;
(6)a.碘水为黄色,三价铁离子也是黄色溶液,滴定过程中需加指示剂,故a错误;
b.滴定过程中,三价铁可以和碘离子发生反应生成亚铁离子和碘单质,碘单质遇到淀粉溶液显示蓝色,不能确定是否达到滴定终点,故b错误;
c.滴定管用蒸馏水洗涤后必须用标准液润洗,故c错误;
d.锥形瓶不需要用待测液润洗,故d正确;
e.滴定过程中,眼睛注视锥形瓶中颜色的变化,故e错误;
f.滴定结束后,30s内溶液不恢复原来的颜色再读数,故f正确.
故答案为:df;
(7)由于所取溶液(含Fe3+)的体积与消耗KI溶液的体积相等,反应的方程式为2Fe3++2I-=2Fe2++I2,结合方程式可知,c(Fe3+)=c(KI)=0.5mol?L-1,所以铁元素的百分含量为:
×100%=70%,
故答案为:70%;
Ⅲ.(8)铁的质量分数是70%,氧元素的质量分数是24%,所以100g铁矿石中,铁元素的质量是70g,氧元素质量是24g,铁元素和氧元素的物质的量比为:
:
=5:6,铁的氧化物的化学式为:Fe5O6,
故答案为:Fe5O6.
故答案为:防止空气中的水蒸气和CO2进入B中,影响测定结果;
(2)测的反应后装置B增重1.35g,根据反应的实质,增加的是氧元素的质量,所以氧元素的质量分数是:
| ||
| 5.0 |
故答案为:24%;
(3)因CO有毒,不能排放到空气中,应加尾气处理装置,故答案为:尾气处理;
Ⅱ.(4)向铁矿石中加入硫酸,酸化反应生成硫酸的铁盐溶液,还存在过量的硫酸溶液,加入过量的氯气,煮沸的作用是赶走溶液中溶解的过量的Cl2,否则会影响与KI的反应,带来实验误差,
故答案为:赶走溶液中溶解的过量的Cl2;
(5)若稀释到250mL,采用的仪器有:烧杯、玻璃棒、胶头滴管、250mL容量瓶,故答案为:250mL容量瓶;
(6)a.碘水为黄色,三价铁离子也是黄色溶液,滴定过程中需加指示剂,故a错误;
b.滴定过程中,三价铁可以和碘离子发生反应生成亚铁离子和碘单质,碘单质遇到淀粉溶液显示蓝色,不能确定是否达到滴定终点,故b错误;
c.滴定管用蒸馏水洗涤后必须用标准液润洗,故c错误;
d.锥形瓶不需要用待测液润洗,故d正确;
e.滴定过程中,眼睛注视锥形瓶中颜色的变化,故e错误;
f.滴定结束后,30s内溶液不恢复原来的颜色再读数,故f正确.
故答案为:df;
(7)由于所取溶液(含Fe3+)的体积与消耗KI溶液的体积相等,反应的方程式为2Fe3++2I-=2Fe2++I2,结合方程式可知,c(Fe3+)=c(KI)=0.5mol?L-1,所以铁元素的百分含量为:
| 0.5mol/L×0.25L×56g/mol |
| 10g |
故答案为:70%;
Ⅲ.(8)铁的质量分数是70%,氧元素的质量分数是24%,所以100g铁矿石中,铁元素的质量是70g,氧元素质量是24g,铁元素和氧元素的物质的量比为:
| 70 |
| 56 |
| 24 |
| 16 |
故答案为:Fe5O6.
点评:本题考查了探究铁矿石中氧元素和铁元素的含量的方法,是一道探究物质的组成、测量物质的含量知识的一道综合考查题,考查学生分析和解决问题的能力,为高考常见题型,综合性强,难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目